题目内容
4.以下有关物质结构的描述正确的是( )| A. | 甲苯分子中的所有原子可能共平面 | B. |  分子中的所有原子可能共平面 分子中的所有原子可能共平面 | ||
| C. | 乙烷分子中的所有原子可能共平面 | D. | 二氯甲烷分子为正四面体结构 |
分析 A.根据甲烷为正四面体结构分析甲苯中所有氢原子能否共平面;
B.根据乙烯和苯分子都是平面机构进行分析;
C.根据甲烷正四面体结构判断乙烷分子的空间结构;
D.由于甲烷中两个氢原子被氯原子取代,C-Cl键与C-H的键长不同,则不属于正四面体结构.
解答 解:A.由于甲烷为正四面体结构,甲苯可以看作甲烷中1个H被苯基取代,所以甲苯中所有原子不可能共平面,故A错误;
B.苯和乙烯都是平面机构,所有原子共平面,则苯乙烯分子中所有原子可以共平面,故B正确;
C.乙烷分子中中含有2个甲基,具有甲烷的四面体结构,则所有原子不可能在同一平面上,故C错误;
D.二氯甲烷中存在两个C-Cl键和2个C-H键,由于它们的键长不同,所以二氯甲烷不可能为正四面体结构,故D错误;
故选B.
点评 本题考查了有机物分子共平面情况判断,题目难度中等,注意掌握常见有机物的结构,明确甲烷、乙烯、乙炔、苯等有机物结构是解题关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
14.类比是研究物质性质的常用方法之一,可预测许多物质的性质.但类比是相对的,不能违背客观实际.下列各说法中,正确的是( )
| A. | IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| B. | CH4是正四面体结构,则SiH4也是正四面体结构 | |
| C. | 锂与氧气反应:4Li+O2═2 Li2O,则钠与氧气反应:4Na+O2═2Na2O | |
| D. | CaCO3与稀硝酸反应生成CO2,则CaSO3与稀硝酸反应生成SO2 |
15.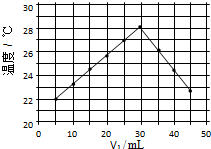 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
 将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )| A. | 做该实验时环境温度为22℃ | |
| B. | 该实验表明化学能可能转化为热能 | |
| C. | NaOH溶液的浓度约为1.5mol/L | |
| D. | 该实验表明有水生成的反应都是放热反应 |
12.下列叙述正确的是( )
| A. | 2s轨道可以和3p轨道形成sp2杂化轨道 | |
| B. | 烯烃中的碳碳双键由l个σ键和l个π键组成 | |
| C. | 由极性键组成的分子,一定是极性分子 | |
| D. | 甲烷中sp3杂化轨道的构型是平面正方形 |
19.下列结论错误的是 ( )
①微粒半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | 只有① | B. | ①③⑤ | C. | ②④⑤⑥⑦ | D. | ②④⑥ |
9.钡在氧气中燃烧时的得到一种钡的氧化物晶体,结构如图所示,有关说法正确的是( ) 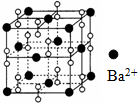

| A. | 该晶体为分子晶体 | |
| B. | 晶体的化学式为Ba2O2 | |
| C. | 该晶体晶胞结构与CsCl相似 | |
| D. | 与每个Ba2+距离相等且最近的Ba2+共有12个 |
16.某有机物的结构简式为 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成 ②水解 ③酯化 ④氧化 ⑤消去.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤消去.
| A. | ①③④ | B. | ①③④⑤ | C. | ②③④ | D. | ①③⑤ |
13.表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素的符号:①N,⑥Si,⑦S.
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性的氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④中,化学性质较活泼的是Na,请设计化学实验加以证明:用钠、镁跟水反应的实验证明:钠可以跟冷水剧烈反应,放出氢气,并生成强碱NaOH,镁跟沸水才反应,放出氢气,并生成中强碱Mg(OH)2.在⑧与⑫中,化学性质较活泼的是Cl,请设计化学实验加以证明:用氯气或氯水与溴化钠溶液反应的实验证明:溶液变为橙色,发生的反应为Cl2+2NaBr═2NaCl+Br2.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅧA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ar
(3)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,称为两性的氢氧化物的是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.
(5)在③与④中,化学性质较活泼的是Na,请设计化学实验加以证明:用钠、镁跟水反应的实验证明:钠可以跟冷水剧烈反应,放出氢气,并生成强碱NaOH,镁跟沸水才反应,放出氢气,并生成中强碱Mg(OH)2.在⑧与⑫中,化学性质较活泼的是Cl,请设计化学实验加以证明:用氯气或氯水与溴化钠溶液反应的实验证明:溶液变为橙色,发生的反应为Cl2+2NaBr═2NaCl+Br2.
 、
、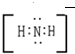 .
.