题目内容
17.下列物质互为同素异形体的是( )| A. | D2O与T2O | B. | 12C与13C | C. | O2与O3 | D. | 乙醇与二甲醚 |
分析 由同种元素形成的不同种单质互为同素异形体,互为同素异形体的物质要符合以下两个条件:同种元素形成,不同单质;据此进行分析判断.
解答 解:判断同素异形体的关键把握两点:①同种元素形成,②不同单质.
A.D2O与T2O是化合物不是单质,不是同素异形体,故A错误;
B.12C与13C是碳元素的不同原子,是碳元素的同位素,不是单质,故B错误;
C.O2与O3都是由氧元素形成的不同物质,都是单质,互为同素异形体,故C正确;
D.乙醇与二甲醚是不同的化合物,属于分子式相同结构不同的物质,属于同分异构体,不是同位素,故D错误;
故选C.
点评 本题难度不大,判断是否互为同素异形体的关键要把握两点:①同种元素形成,②不同单质,这是解决此类题的关键之所在.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
7.分子式为C4H10O2的同分异构体中,只有一种官能团且能与钠反应的共有(已知:同一个碳上连有多个羟基不
稳定)( )
稳定)( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
8.下列离子方程式正确的是( )
| A. | 过氧化钠固体与水反应:2O22-+2H2O═OH-+O2↑ | |
| B. | MnO2与浓盐酸反应制Cl2:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl-+Cl2↑+2H2O | |
| C. | 稀硝酸与过量的铁屑反应Fe+4H-+NO3-═Fe3++NO↑+2H2O | |
| D. | NaAlO2溶液中通入过量二氧化碳AlO2-+2H2O+CO2═HCO3-+Al(OH)3↓ |
5.分枝酸结构简式如图,下列说法正确的是( )


| A. | 分子式为C10H8O6 | |
| B. | 分子中含有3种官能团 | |
| C. | 可与乙醇、乙酸反应,且反应类型相同 | |
| D. | 1mol分枝酸最多可与3mol NaOH发生中和反应 |
12.锂原子比镁原子少1个电子层,最外层电子数也比镁原子少1,在周期表中锂和镁的位置关系存在有“对角线”关系,“对角线”关系的元素性质存在相似性.下列关于锂的判断可能正确的是( )
| A. | Li能在空气中燃烧 | B. | Li2O熔点较低 | ||
| C. | Li2CO3能溶于水 | D. | LiOH受热时易分解 |
2.下列物质中,属于共价化合物的是( )
| A. | Cl2 | B. | NH4Cl | C. | C2H6 | D. | KOH |
9.下列有关说法正确的是( )
| A. | 铅蓄电池放电时,正极和负极的电极质量均增大 | |
| B. | 反应Cl2(g)+H2O(1)=HCl(aq)+HClO(aq)在常温下能自发进行,则该反应的△H<0 | |
| C. | 在N2(g)+3H2(g)?2NH3(g)平衡体系中加入催化剂,N2的反应速率和转化率均增大 | |
| D. | C2H5Br水解生成乙醇(△H>0),加入少量NaOH浓溶液并加热,该化学反应速率增大其平衡常数不变 |
6.下列关于烷烃性质的叙述正确的是( )
| A. | 烷烃分子中碳原子不可能在同一平面上 | |
| B. | 烷烃易被酸性高锰酸钾溶液氧化 | |
| C. | 在光照条件下,烷烃易与溴水发生取代反应 | |
| D. | 烷烃的卤代反应很难得到纯净的产物 |
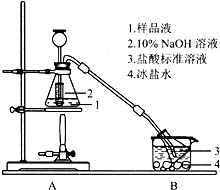 Cux(NH3)y(SO4)z•nH2O是深蓝色晶体,可溶于水,不溶于乙醇、乙醚等有机溶剂,常用作杀虫剂、媒染剂等.某小组利用废铜屑、硫酸、氨水等原料制备该晶体并测定其组成.
Cux(NH3)y(SO4)z•nH2O是深蓝色晶体,可溶于水,不溶于乙醇、乙醚等有机溶剂,常用作杀虫剂、媒染剂等.某小组利用废铜屑、硫酸、氨水等原料制备该晶体并测定其组成.