题目内容
2.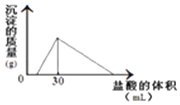 将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为2.016L(标准状况)
将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为2.016L(标准状况)
分析 由图可知加入盐酸不与立刻生成沉淀,说明盐酸先中和氢氧化钠,故合金全部溶解所得溶液为氢氧化钠与偏铝酸钠混合溶液,溶液中n(Na+)=n(OH-)+n(AlO2-),当加入盐酸30mL时,沉淀量最大,此时溶液为氯化钠溶液,根据氯元素守恒有n(NaCl)=n(HCl),根据钠元素守恒有n(NaCl)=n(Na)=n(Na+),PH=14的溶液中c(OH-)=1mol/L,计算n(AlO2-),n(Al)=n(AlO2-),根据电子转移守恒计算n(H2),再根据V=nVm计算氢气体积.
解答 解:由图可知加入盐酸不与立刻生成沉淀,说明盐酸先中和氢氧化钠,故合金全部溶解所得溶液为氢氧化钠与偏铝酸钠混合溶液,溶液中n(Na+)=n(OH-)+n(AlO2-),当加入盐酸30mL时,沉淀量最大,此时溶液为氯化钠溶液,根据氯元素守恒有n(NaCl)=n(HCl)=0.03L×2mol/L=0.06mol,根据钠元素守恒有n(NaCl)=n(Na)=n(Na+)=0.06mol,pH=14的溶液中c(OH-)=1mol/L,含有氢氧根离子的物质的量为:n(OH-)=0.02L×1mol/L=0.02mol,
所以n(AlO2-)=0.06mol-0.02mol=0.04mol,所以n(Al)=n(AlO2-)=0.04mol,根据电子转移守恒可知:n(H2)×2=n(Na)×1+n(Al)×3,即2n(H2)=0.06mol+0.04mol×3=0.18mol,解得:n(H2)=0.09mol,
生成氢气在标况下的体积为:V(H2)=0.09mol×22.4L/mol=2.016L,
故答案为:2.016.
点评 本题考查混合物反应的计算,题目难度中等,明确发生反应的实质为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

| A. | CH3COOH有酸性,而醇、酮类物质没有酸性 | |
| B. | 甲苯使酸性高锰酸钾褪色,而苯不能使其褪色 | |
| C. | 苯酚遇铁离子发生显色反应,而醇不能 | |
| D. | 乙醛与HCN发生加成反应,乙烯不能与之加成 |
| A. | 该反应的氧化剂是ClO- | |
| B. | 该反应中有两种离子生成 | |
| C. | 参加反应的氧化剂与还原剂的物质的量之比为2:3 | |
| D. | 该反应消耗1mol还原剂时,转移的电子为3 mol |
| A. | 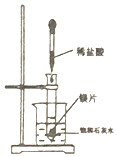 利用图装置,可以研究Ca(OH)2的溶解度随温度的变化 | |
| B. | 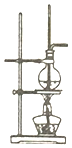 利用图装置,可以利用乙醇制备乙烯 | |
| C. |  利用图装置,可以利用生石灰和NH4C1固体制NH3 | |
| D. | 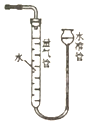 利用图装置,可以测定浓硝酸与铜反应生成的NO2气体体积 |
| A. | 在5NH4NO3═2HNO3+4N2↑+9H2O中,生成56g N2时转移电子的数目为15×6.02×1023 | |
| B. | 16.2 g纤维素完全燃烧,产生CO2分子的物质的量约为0.6mol | |
| C. | 铅蓄电池放电一段时间后,负极质量减小,正极质量增加 | |
| D. | 向水中加入NaHCO3或NaHSO3固体后,水的电离程度均增大 |

| A. | 同分异构体 | B. | 同素异形体 | C. | 同位素 | D. | 同系物 |
| A. | ${\;}_{6}^{12}$C和${\;}_{6}^{13}$C | B. | H2O和D2O | ||
| C. | O2与O3 | D. | CH3OCH3与CH3CH2OH |
| A. | 使用含微量NaF的牙膏,可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F以防止蛀牙,则一般可说明后者的Ksp小于前者的Ksp | |
| B. | 室温下向苯和含少量苯酚杂质的混合溶液中加入适量浓溴水,振荡,静置后过滤,可除去苯中少量苯酚杂质 | |
| C. | 用1.00mol/L 标准盐酸滴定未知浓度的NaOH溶液10.00mL,滴定前将25.00mL 酸式滴定管中盐酸调至“0”刻度,将盐酸滴完恰好滴定至终点,则可得c(NaOH)=2.50mol/L | |
| D. | 向4ml 2%的CuSO4溶液中加入几滴1%的NaOH溶液,振荡后再加入0.5mL 有机物X,加热后未出现砖红色沉淀,说明X结构中不含有醛基 |