题目内容
4.下列说法正确的是( )| A. | 在5NH4NO3═2HNO3+4N2↑+9H2O中,生成56g N2时转移电子的数目为15×6.02×1023 | |
| B. | 16.2 g纤维素完全燃烧,产生CO2分子的物质的量约为0.6mol | |
| C. | 铅蓄电池放电一段时间后,负极质量减小,正极质量增加 | |
| D. | 向水中加入NaHCO3或NaHSO3固体后,水的电离程度均增大 |
分析 A.反应中部分硝酸根中N元素由+5价降低为氮气中0价,铵根中N元素-3价升高为氮气中0价,氮气既是还原产物又是氧化产物,由氮原子守恒,结合方程式可知,还原产物与氧化产物物质的量之比为3:5,根据n=$\frac{m}{M}$计算氮气物质的量,再计算氧化产物物质的量,再结合铵根中N元素化合价变化计算转移电子物质的量;
B.纤维素的最简式为C6H10O5,求出纤维素中含有的C6H10O5的物质的量,然后根据碳守恒判断燃烧生成的二氧化碳物质的量;
C.放电时负极反应为Pb-2e-+SO42-═PbSO4,正极反应为PbO2+4H++SO42-+2e-═PbSO4+2H2O;
D.酸溶液和碱溶液抑制了水的电离,能够水解的盐溶液促进了水的电离,NaHSO3溶液中HSO3-的电离程度大于水解程度.
解答 解:A.反应中部分硝酸根中N元素由+5价降低为氮气中0价,铵根中N元素-3价升高为氮气中0价,氮气既是还原产物又是氧化产物,由氮原子守恒,结合方程式可知,还原产物与氧化产物物质的量之比为3:5,生成氮气物质的量为$\frac{56g}{28g/mol}$=2mol,故氧化产物的物质的量为2mol×$\frac{5}{8}$=$\frac{5}{4}$mol,铵根中N元素被氧化,故转移电子为$\frac{5}{4}$mol×2×[0-(-3)]=7.5mol,故A错误;
B.纤维素(C6H10O5)n,纤维素的最简式为C6H10O5,16.2g纤维素中含有的C6H10O5的物质的量为0.1mol,而1molC6H10O5燃烧生成6mol二氧化碳,故0.1molC6H10O5燃烧生成0.6mol二氧化碳,故B正确;
C.放电时负极发生Pb-2e-+SO42-═PbSO4,负极质量增加,正极上是二氧化铅得电子,都是生成硫酸铅,正极质量也增加,故C错误;
D.NaHCO3为强碱弱酸盐,碳酸氢根离子的水解,促进了水的电离,HSO3-的水解程度大于其电离程度,相当于一元弱酸,抑制水的电离,故D错误;
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算、电化学、盐类的水解等知识,注意掌握公式的运用和物质的性质,A选项有关氧化还原反应计算,关键是判断反应中N元素化合价变化,为易错点,题目难度中等.

| A. | 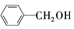 酚类-OH 酚类-OH | B. | 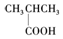 羧酸-CHO 羧酸-CHO | C. | 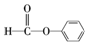 醛类-CHO 醛类-CHO | D. | CH3-O-CH3 醚类  |
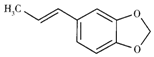 黄樟脑(结构简式如图)可作为洋茉莉和香兰素的原料,能除肥皂的油脂臭,常作廉价的香料使用于皂用香精中.下列有关叙述正确的是( )
黄樟脑(结构简式如图)可作为洋茉莉和香兰素的原料,能除肥皂的油脂臭,常作廉价的香料使用于皂用香精中.下列有关叙述正确的是( )| A. | 黄樟脑属于酯、烯烃、芳香族化合物 | |
| B. | 黄樟脑分子中最少有9个碳原子共面 | |
| C. | 黄樟脑与H2、Br2均能发生加成反应 | |
| D. | 与黄樟脑互为同分异构体且含苯环、羧基及一个支链的结构有3种 |
| A. |  分离碘酒中的碘和酒精 | |
| B. |  分离沸点相差较大的互溶混合物 | |
| C. |  制取氯化镁固体 | |
| D. |  检验蔗糖与浓硫酸反应产生的二氧化碳 |
| A. | 1 mol CnH2n-2(n≥2)中所含的共用电子对数为(3n+1)NA | |
| B. | 25℃时,1L pH=2 的H2SO4溶液中所含H+数为0.01NA | |
| C. | 标准状况下,22.4 L CH3OH 中含有的共价键数为5NA | |
| D. | 60g的乙酸和葡萄糖混合物充分燃烧消耗3NA个O2 |
| A. | CH2=CH-CH2Cl | B. | CH2=CH-COOH | C. | CH3-CH(OH)-COOH | D. | H2N-CH2-COOH |
| A. | 陶瓷是中华民族祖先的一项伟大发明,烧结黏土制陶瓷的过程不涉及化学反应 | |
| B. | 制作烟花的过程中常加入金属发光剂和发色剂使烟花放出五彩缤纷的颜色 | |
| C. | “水滴石穿”主要是溶解了的雨水对石灰石的溶解作用 | |
| D. | 严格地讲通风橱”是一种不负责任的防污染手段,因为实验产生的有害气体没有得到转化或吸收 |
| A. | 由石油制取乙烯、丙烯等化工原料不涉及化学变化 | |
| B. | 向牛奶中加入果汁会产生沉淀,这是因为发生了酸碱中和反应 | |
| C. | 鲜花运输途中需喷洒高锰酸钾稀溶液,主要是为鲜花补充钾肥 | |
| D. | 牙膏中添加的Na3PO3F、NaF提供的氟离子浓度相等时,它们防治龋齿的作用相同 |
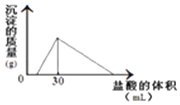 将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为2.016L(标准状况)
将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如图:则反应过程中产生氢气的总体积为2.016L(标准状况)