题目内容
20.下列溶液pH一定等于1的是( )| A. | 25℃1L的0.1mol•L-1H2SO4溶液 | |
| B. | T℃1L 0.2mol•L-1H2SO4溶液中加入1L 0.2mol•L-1NaOH溶液后得到的2L溶液 | |
| C. | 25℃a mol•L-1NaHSO4溶液[已知50ml amol•L-1Ba(OH)2溶液与100mL amol•L-1NaHSO4溶液混合后pH=7] | |
| D. | T℃c(OH-)=10-13mol•L-1的某盐溶液 |
分析 溶液的pH=1,则混合液中氢离子浓度为0.1mol/L,
A.0.1mol/L的硫酸溶液中氢离子浓度为0.2mol/L;
B.硫酸为二元酸,混合液中硫酸过量,根据题中数据计算出氢离子的物质的量及浓度;
C.无法计算溶液中氢离子浓度;
D.温度影响水的离子积,不是常温下,无法计算溶液中氢离子浓度.
解答 解:A.25℃1L的0.1mol.L-1H2SO4溶液中氢离子浓度为0.2mol/L,溶液的pH=lg0.2<1,故A正确;
B.T℃1L 0.2mol.L-1H2SO4溶液中加入1L 0.2mol.L-1NaOH溶液后得到的2L溶液,混合液中氢离子浓度为:$\frac{0.2mol/L×2×1L-0.2mol/L×1L}{2L}$=0.1mol/L,反应后溶液的pH为1,故B正确;
C.25℃a mol•L-1NaHSO4溶液中氢离子浓度为amol/L,不一定为0.1mol/L,则无法计算溶液的pH,故C错误;
D.T℃c(OH-)=10-13mol•L-1的盐溶液中,c(H+)=$\frac{{K}_{w}}{c(O{H}^{-})}$,由于温度影响水的离子积Kw,题中没有告诉在常温下,则该溶液中氢离子浓度不一定为0.1mol/L,故D错误;
故选A.
点评 本题考查了溶液pH的计算与判断,题目难度中等,明确溶液酸碱性与溶液pH的关系及计算方法为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
8.下列图片与其相关描述正确的共有( )

①图1为闻气体时的正确操作
②图2为单质硅的用途之一
③图3为浓硫酸的罐车上所贴的危险化学品标识
④图4反应A(g)+B(g)=C(g)+D(g)为吸热反应
⑤图5为按元素相对原子质量制出第一张元素周期表的俄国化学家门捷列夫纪念币.

①图1为闻气体时的正确操作
②图2为单质硅的用途之一
③图3为浓硫酸的罐车上所贴的危险化学品标识
④图4反应A(g)+B(g)=C(g)+D(g)为吸热反应
⑤图5为按元素相对原子质量制出第一张元素周期表的俄国化学家门捷列夫纪念币.
| A. | 1组 | B. | 2组 | C. | 3组 | D. | 4组 |
5.下列各种冶炼方法中,可制得相应金属的是( )
| A. | 加热Al2O3 | B. | 加热CaCO3 | ||
| C. | 电解熔融NaCl | D. | 氰化钠与铝粉高温共热 |
9.NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mo1•L-1 | |
| B. | 标准状况下,22.4L水所含的分子数为NA | |
| C. | 常温常压下NO2和N2O4混合气体22.4L,其中含有的原子总数为0.3NA | |
| D. | 常温下,4gCH4含有NA个C-H共价键 |
10.据诺贝尔奖委员会官方网站报道,2012年度诺贝尔化学奖已经于北京时间2012年10月10日17:45公布,由于在“G蛋白偶联受体”方面所作出的突破性贡献,2012年的化学奖项授予美国科学家( )以及布莱恩•克比尔卡.
| A. | 罗伯特•洛夫科维茨 | B. | 丹•谢赫特曼 | ||
| C. | 理查德•赫克 | D. | 托马斯•施泰茨 |





 短周期主族元素A、B、C、D、E、F的原子序数依次增大,已知A的原子半径比B的小,B在反应中既不容易得到电子也不容易失去电子,C元素的气态氢化物和其最高价氧化物对应水化物能化合生成盐,元素D的原子最外层电子数是其电子层数的3倍,E与A同一主族,F常用于制半导体.
短周期主族元素A、B、C、D、E、F的原子序数依次增大,已知A的原子半径比B的小,B在反应中既不容易得到电子也不容易失去电子,C元素的气态氢化物和其最高价氧化物对应水化物能化合生成盐,元素D的原子最外层电子数是其电子层数的3倍,E与A同一主族,F常用于制半导体.
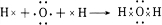 ,写出A2D与X反应的化学方程式,并用单线桥标出电子转移
,写出A2D与X反应的化学方程式,并用单线桥标出电子转移