题目内容
8.下列图片与其相关描述正确的共有( )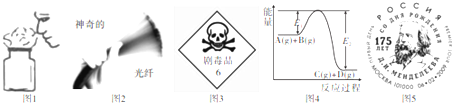
①图1为闻气体时的正确操作
②图2为单质硅的用途之一
③图3为浓硫酸的罐车上所贴的危险化学品标识
④图4反应A(g)+B(g)=C(g)+D(g)为吸热反应
⑤图5为按元素相对原子质量制出第一张元素周期表的俄国化学家门捷列夫纪念币.
| A. | 1组 | B. | 2组 | C. | 3组 | D. | 4组 |
分析 ①闻气体应利用手轻轻扇动,使极少量气体进入鼻孔;
②光纤的成分为二氧化硅;
③浓硫酸不是剧毒物质,具有强烈的腐蚀性;
④反应物的总能量高;
⑤1865年,俄国化学家门捷列夫制出第一张元素周期表.
解答 解:①闻气体应利用手轻轻扇动,使极少量气体进入鼻孔,操作错误,故不选;
②光纤的成分为二氧化硅,而不是Si,故不选;
③浓硫酸不是剧毒物质,具有强烈的腐蚀性,所贴的危险化学品标识不合理,故不选;
④反应物的总能量高,则该反应为放热反应,故不选;
⑤1865年,俄国化学家门捷列夫制出第一张元素周期表,该图正确,故选;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验操作、物质的性质、实验安全及化学史等,把握实验操作、实验技能及相关反应原理为解答本题的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
16.液氨与水相似,也存在着微弱的自偶电离:2NH3?NH4++NH2-.对该体系的说法中错误的是( )
| A. | 一定温度下,液氨中c(NH4+)与c(NH2-)的乘积为一常数 | |
| B. | 只要不加入其他物质,液氨中c(NH4+)总是与c(NH2-)相等 | |
| C. | 液氨的电离达到平衡时,c(NH3)=c(NH2-)=c(NH4+) | |
| D. | 液氨中含有NH3、NH4+和NH2- |
3.现有部分短周期元素的性质与原子(或分子)结构如下表:
(1)W在周期表中位于第二周期第VIA主族;元素Y与元素Z相比,金属性较强的是Na(用元素符号表示).下列表述中能证明这一事实的是cd(填序号).
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.单质Y能与冷水剧烈反应而Z不能
d.最高价氧化物对应的水化物碱性YOH强于Z(OH)2
(2)上述元素可形成含有共价键的二元离子化合物(包含两种不同元素的离子化合物),该化合物的化学式为Na2O2,该物质中阴阳离子个数比为1:2.
(3)W、X的氢化物H2W2、X2H4在一定条件下反应可得到一种在空气中体积分数最大的单质与常温下为液体的物质,写出该反应的化学方程式:2H2O2+N2H4=N2+4H2O.
| 元素符号 | W | X | Y | Z |
| 原子消息 | 海水中质量分数最高的元素 | 非金属性强而单质(X2)很稳定 | M层比K层少1个电子 | 第三周期元素的简单离子中半径最小 |
a.Y单质的熔点比Z单质低
b.Y的化合价比Z低
c.单质Y能与冷水剧烈反应而Z不能
d.最高价氧化物对应的水化物碱性YOH强于Z(OH)2
(2)上述元素可形成含有共价键的二元离子化合物(包含两种不同元素的离子化合物),该化合物的化学式为Na2O2,该物质中阴阳离子个数比为1:2.
(3)W、X的氢化物H2W2、X2H4在一定条件下反应可得到一种在空气中体积分数最大的单质与常温下为液体的物质,写出该反应的化学方程式:2H2O2+N2H4=N2+4H2O.
13.利用如图所示装置进行下列实验,试管c中现察到的实验现象正确的是( )
| 选项 | a | b | c | 实验现象 |  |
| A | 浓盐酸 | MnO2 | 品红溶液 | 品红褪色 | |
| h | 硫酸 | NaHCO3 | Na2SiO3 | 有白色色胶状沉淀产生 | |
| r | 浓氨水 | 生石灰 | AlCl3溶液 | 白色沉淀生成,后沉淀消失 | |
| D | 70%H2SO4 | Na2SO3 | 紫色石蕊溶液 | 溶液先变红.后褪色 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
20.下列溶液pH一定等于1的是( )
| A. | 25℃1L的0.1mol•L-1H2SO4溶液 | |
| B. | T℃1L 0.2mol•L-1H2SO4溶液中加入1L 0.2mol•L-1NaOH溶液后得到的2L溶液 | |
| C. | 25℃a mol•L-1NaHSO4溶液[已知50ml amol•L-1Ba(OH)2溶液与100mL amol•L-1NaHSO4溶液混合后pH=7] | |
| D. | T℃c(OH-)=10-13mol•L-1的某盐溶液 |
18.下列热化学方程式正确的是( )
| A. | 甲烷的燃烧热为890.3kJ•mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3KJ•mol-1 | |
| B. | 500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ•mol-1 | |
| C. | 已知在120℃,101kPa下,1gH2燃烧生成水蒸气放出121kJ热量,其热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-242kJ•mol-1 | |
| D. | 25℃,101Kpa时,强酸与强碱的稀溶液发生反应的中和热为57.3kJ•mol-1,硫酸稀溶液与氢氧化钾稀溶液反应的热化学方程式可表示为:H2SO4(aq)+2KOH(aq)═K2SO4(aq)+2H2O(1)△H=-114.6kJ•mol-1 |