��Ŀ����
9�� ��Ȼ����ڷḻ��̼�������衢�ס�����Ԫ�أ����ǿ��γɵ��ʼ���������Ҫ��ش��������⣺
��Ȼ����ڷḻ��̼�������衢�ס�����Ԫ�أ����ǿ��γɵ��ʼ���������Ҫ��ش��������⣺��1��������CO�γ������Fe��CO��5�����۵�Ϊ-20.50C���е�Ϊ1020C��������CCl4���ݴ��ж�Fe��CO��5�������ڷ��Ӿ��壨������ͣ���
��2������Ԫ�����ڱ���λ���ǵ������ڵڢ��壬�������Ӿ���ǿ��ԭ�ԣ��ӵ����Ų��ĽǶȽ��ͣ���ԭ����Fe2+��3d�����6�����ӣ�ʧȥ1�����Ӻ�3d��������Ų����ڰ�����ȶ�״̬��
��3���Ϻ������̲��Ŵ�������Ȼ��ˮ������׳ơ���ȼ��������ȼ����һ�־��壬������ƽ��ÿ46��H2O����ͨ���������8������ÿ�����ڿ�����1��CH4���ӻ�1�������H2O���ӣ���������ÿ8������6��������CH4���ӣ�����2�����������H2O������䣮��ȼ����ƽ����ɿɱ�ʾΪCH4•8H2O��
��4�������ᣨH3PO3�����NaOH��Ӧ��ַ�Ӧ��������������ƣ�Na2HPO3��������������������������Σ������������ʽ������
��5�����ʯ�����ṹģ����ͼ������BN�ṹ����ʯ���ƣ�Ӳ������ʯ�൱��������BN�����У�Bԭ����Nԭ��֮�乲�ۼ�����λ������Ŀ��Ϊ3��1��ÿ��Nԭ����Χ����ҵȾ����Nԭ����Ϊ12���������ӵ���������ȡ6��1023/mol������BN���ܶ�Ϊa g•cm-3��Ħ������Ϊb g•mol-1�����㾧�������������Nԭ�Ӽ������$\frac{\sqrt{2}}{2}\root{3}{\frac{b}{150a}}$nm���ú�a��b����ʽ��ʾ����
���� ��1������Fe��CO��5���۷е�ͣ������������Ȼ�̼�жϾ������ͣ�
��2������ԭ������Ϊ26�������ڱ��д��ڵ������ڵ�VIII�壻����������Ӻ������ӵĵ����Ų�ʽ�����жϣ�
��3���ڡ���ȼ���������У�ÿ8������46��H2O���ӹ��ɿ�ܣ���������6��CH4���Ӻ�2��H2O���ӣ����ж�ÿ8������48��H2O���Ӻ�6��CH4���ӣ��ݴ��ƶϿɱ�ʾ��ȼ����ƽ����ɵĻ�ѧʽ��
��4��H3PO3�����NaOH��Ӧ��ַ�Ӧ��������������ƣ�Na2HPO3����������������ƣ�Na2HPO3�������Ե���������ӣ�
��5���ɽ��ʯ�ľ����ṹ��֪�������ڲ���4��Cԭ�ӣ���������6��Cԭ�ӣ�������8��Cԭ�ӣ����ݽ��ʯ�Ľṹ�жϣ���BN�����У�ÿ��Bԭ�Ӻ�4��Nԭ���γɹ��ۼ���Bԭ�ӵ���λ����4��Bԭ����Nԭ��֮�乲�ۼ�����Ŀ��12��һ��������Nԭ����ĿΪ4�����ݾ����ṹͼ���Ծ��������ϵĵ�ԭ��Ϊ������õ�ԭ�Ӿ�������ĵ�ԭ��λ�ھ����ö������������ϣ�����$��=\frac{m}{��}$�ɼ�������������������ȷ�������ı߳������������Nԭ�Ӽ�����Ǿ�����Խ��ߵ�$\frac{1}{2}$���ݴ˼��㣻
��� �⣺��1��Fe��CO��5���۷е�ͣ������������Ȼ�̼�����ݷ��Ӿ����۷е�ͣ��Ҵ�����������ԭ������֪Fe��CO��5Ϊ���Ӿ��壻
�ʴ�Ϊ�����Ӿ��壻
��2����Ϊ26��Ԫ�أ�Ԫ�������ڱ���λ�ڵ������ڢ��壻����Fe2+�ļ۵���3d6ʧȥһ�����ӿ��γ�3d5������ȶ��ṹ������Fe2+�ױ�������Fe3+��
�ʴ�Ϊ���������ڢ��壻Fe2+ ��3d�����6�����ӣ�ʧȥ1�����Ӻ�3d��������Ų����ڰ�����ȶ�״̬��
��3��������8����ֻ��6������CH4���ӣ�����2������ˮ������䣬�Ƴ�8��������6��������ӣ�46+2=48��ˮ���ӣ�����������ˮ���ӵĸ���֮��=6��48=1��8�����Ի�ѧʽΪCH4•8H2O��
�ʴ�Ϊ��CH4•8H2O��
��4��H3PO3�����NaOH��Ӧ��ַ�Ӧ��������������ƣ�Na2HPO3����������������ƣ�Na2HPO3�������Ե���������ӣ�Ϊ���Σ�
�ʴ�Ϊ�����Σ�
��5���ɽ��ʯ�ľ����ṹ��֪�������ڲ���4��Cԭ�ӣ���������6��Cԭ�ӣ�������8��Cԭ�ӣ���BN�����У�ÿ��Bԭ�Ӻ�4��Nԭ���γɹ��ۼ���Bԭ�ӵ���λ����4��Bԭ����Nԭ��֮�乲�ۼ�����Ŀ��12������Bԭ����Nԭ��֮�乲�ۼ�����Ŀ����λ������Ŀ��Ϊ 3��1�����ݾ����ṹͼ���Ծ��������ϵĵ�ԭ��Ϊ������õ�ԭ�Ӿ�������ĵ�ԭ��λ�ھ����ö������������ϣ�������ԭ����12�������ݾ�̯��֪��һ��������Nԭ����ĿΪ 4��Bԭ����ĿҲ��4������$��=\frac{m}{V}$��֪���������V=$\frac{\frac{4b}{6��10{\;}^{23}}}{a}$cm3=$\frac{4b}{6��10{\;}^{23}a}$cm3�����Ծ����ı߳�Ϊ$\root{3}{\frac{4b}{6��1{0}^{23}a}}$cm�����������Nԭ�Ӽ�����Ǿ�����Խ��ߵ�$\frac{1}{2}$�����Ծ��������������Nԭ�Ӽ������$\frac{1}{2}��\sqrt{2}��$$\root{3}{\frac{4b}{6��1{0}^{23}a}}$cm=$\frac{\sqrt{2}}{2}\root{3}{\frac{4b}{6��1{0}^{23}a}}$cm=$\frac{\sqrt{2}}{2}\root{3}{\frac{b}{150a}}$nm��
�ʴ�Ϊ��3��1��12��$\frac{\sqrt{2}}{2}\root{3}{\frac{b}{150a}}$��
���� ���⿼���˽������ʼ��仯������ۺ�Ӧ�á�����ṹ�����ʡ����������֪ʶ����Ŀ�Ѷ��еȣ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ���ѧ���ķ������������������Ӧ��������ע�����ճ����������ʼ��仯��������ʣ���ȷ��̯���ھ��������е�Ӧ�ã�

| ʵ����������� | ʵ����� | |
| ����һ | ���ù���ȫ�������ڵ���ɫ��Һ�� | �϶���Cu2+�� |
| ����� | ��������Һ�м����������ᣬ������ɫ��ζ�����干�ռ���2.24L����״������ | �϶���CO32- �϶���Ba2+ |
| ������ | �����������Һ�м�����������BaCl2��Һ���������������˲�ϴ�Ӹ�����46.6g��ɫ������ | �϶���SO42- |
| ������ | ������������Һ�м���AgNO3��Һ���ð�ɫ������ |
��2��ԭ�����к���Na+����������Һ�ʵ����ԣ������������ӣ��Ƿ���Cl-��˵������̼����������������֮��Ϊ39g���������ӣ�

| A�� | ��ʵ����������̹��漰6����ѧ��Ӧ | |
| B�� | ��ʵ�����������ֻ�漰1��������ԭ��Ӧ | |
| C�� | �������һ����Al����NH4��2SO4��MgCl2��һ��û��AlCl3��FeCl3 | |
| D�� | �������һ����Al����NH4��2SO4��MgCl2��AlCl3��һ��û��FeCl3 |
 ���������ش����������ƺͶ��ȷ�
���������ش����������ƺͶ��ȷ� �ķ�ˮ������ԭ����ͼ��ʾ������˵��������ǣ�������
�ķ�ˮ������ԭ����ͼ��ʾ������˵��������ǣ�������| A�� | �缫b������ | B�� | ���Ӵ�b������a�� | ||
| C�� | ������ķ�ˮpH���� | D�� | a���ĵ缫��Ӧʽ�� +2e-+H+�T +2e-+H+�T +Cl- +Cl- |

| A�� | �������������� | |
| B�� | ������Ķ��ȴ���������ͬ���칹�� | |
| C�� | ��������ͨ������������� | |
| D�� | ��������������ʹ����KMnO4��Һ��ɫ |
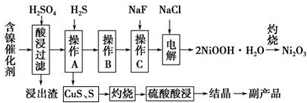 Ϊ�������÷�����������Ҫ�ɷ�ΪNiO������Fe2O3��CaO��CuO��BaO�ȣ���������Ա������һ�ֻ��������¹��գ�����������ͼ��
Ϊ�������÷�����������Ҫ�ɷ�ΪNiO������Fe2O3��CaO��CuO��BaO�ȣ���������Ա������һ�ֻ��������¹��գ�����������ͼ��| �������� | Fe��OH��3 | Fe��OH��2 | Ni��OH��2 |
| ��ʼ������pH | 1.5 | 6.5 | 7.7 |
| ������ȫ��pH | 3.7 | 9.7 | 9.2 |
��pH���ұ� ��Cu2O+2H+=Cu+Cu2++H2O
�۳���ʱ��Ksp��CaF2��=2.7��10-11
�ش��������⣺
��1��д�����ʱFe2O3�����ᷴӦ�Ļ�ѧ����ʽFe2O3+3H2SO4=Fe2��SO4��3+3H2O��
��2����������Ҫ�ɷ�ΪCaSO4•2H2O��BaSO4�������ʣ�
��3������B�dz�ȥ��Һ�е���Ԫ�أ�ijͬѧ��������·����������A���õ���Һ�м���NaOH��Һ��������ҺpH��3.7��7.7��Χ�ڣ����ã����ˣ���Ը�ʵ�鷽���������۷��������ڵ���pHǰ��Ӧ������Һ�м���H2O2��ʹ��Һ�е�Fe2+����ΪFe3+����ԭ������ȷ����˵�����ɣ���ԭ������������Ը�������
��4�������еġ�����Ʒ��ΪCuSO4•5H2O���ѧʽ�����ڿ���������CuS���Եõ�ͭ���������Cu��Cu2O��CuO��ɵĻ�����м���1L 0.6mol•L-1HNO3��Һǡ��ʹ������ܽ⣬ͬʱ�ռ���2240mLNO���壨��״���������û�����к�0.1molCu����ϡ�����ַ�Ӧ��������0.1mol H2SO4��
��5������C��Ϊ�˳�ȥ��Һ�е�Ca2+����������Һ��F-Ũ��Ϊ3��10-3mol•L-1������Һ��$\frac{c��C{a}^{2+}��}{c��{F}^{-}��}$=1.0��10-3��
��6��������2NiOOH•H2O��ԭ����������
�ټ��������£�Cl-������������ΪClO-���������ĵ缫��ӦʽΪCl-+2OH--2e-=ClO-+H2O��
��Ni2+��ClO-��������2NiOOH•H2O��������ò���Ӧ�����ӷ���ʽΪClO-+2Ni2++4OH-=2NiOOH•H2O��+Cl-��
| A�� | ����ʱ������ƿ��Һ���������ܳ����ݻ���$\frac{2}{3}$��Һ��Ҳ�������� | |
| B�� | ���Թ��е�Һ�����ʱҪ��ʱ�ƶ��Թܣ����Ⱪ�� | |
| C�� | ����ϡ�������MgI��AgNO3��Na2CO3��NaAlO2������Һ | |
| D�� | ϡ��Ũ����ʱ��������з������֣�����ˮ��������װ��Ũ������ձ��� |

| A�� | �÷�Ӧ�ɱ�ʾΪ��2A��g��+B��g��?C��g����H��0 | |
| B�� | t��ʱ�÷�Ӧ��ƽ�ⳣ��K=6.25 | |
| C�� | �������������ܶȲ��ٱ仯ʱ���÷�Ӧ�ﵽƽ��״̬ | |
| D�� | t�棬�ڵ�6 minʱ������ϵ�г���0.4 mol C���ٴδﵽƽ��ʱC�������������0.25 |
| A�� | CH3COO-+H2O?CH3COOH+OH- | B�� | Al3++H2O?Al��OH��3+H+ | ||
| C�� | CH3COOH+NaOH?CH3COONa+H2O | D�� | NaCl+H2O?NaOH+HCl |