题目内容
五种短周期元素在周期表中的相对位置如下所示,其中X元素原子核外电子总数是其电子层数的3倍.
请回答下列问题:
(1)请写出元素符号:X Y W
(2)元素Z位于周期表中第 周期 族;
(3)M的氢化物的电子式为 ;
(4)Y的最高价氧化物水化物为 ,属于 酸.(填“强”或“弱”)
| X | Y | ||
| Z | W | M |
(1)请写出元素符号:X
(2)元素Z位于周期表中第
(3)M的氢化物的电子式为
(4)Y的最高价氧化物水化物为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由短周期元素在周期表中的相对位置可知,X、Y处于第二周期,Z、W、M处于第三周期,其中X元素原子核外电子总数是其电子层数的3倍,则X核外电子数为6,故X为C元素,可推知Y为N、Z为P、W为S、M为Cl,据此解答.
解答:
解:由短周期元素在周期表中的相对位置可知,X、Y处于第二周期,Z、W、M处于第三周期,其中X元素原子核外电子总数是其电子层数的3倍,则X核外电子数为6,故X为C元素,可推知Y为N、Z为P、W为S、M为Cl,
(1)由上述分析可知:X为C、Y为N、W为S,故答案为:C;N;S;
(2)Z为P元素,位于周期表中第三周期VA族,故答案为:三、VA;
(3)M为Cl元素,其氢化物为HCl,电子式为 ,故答案为:
,故答案为: ;
;
(4)Y为N元素,最高价氧化物水化物为HNO3,属于强酸,故答案为:HNO3;强.
(1)由上述分析可知:X为C、Y为N、W为S,故答案为:C;N;S;
(2)Z为P元素,位于周期表中第三周期VA族,故答案为:三、VA;
(3)M为Cl元素,其氢化物为HCl,电子式为
 ,故答案为:
,故答案为: ;
;(4)Y为N元素,最高价氧化物水化物为HNO3,属于强酸,故答案为:HNO3;强.
点评:本题考查元素周期表、结构与位置关系等,难度不大,侧重对基础知识的巩固.

练习册系列答案
相关题目
设阿伏伽德罗常数为NA,下列说法正确的是( )
| A、1.8g重水(D2O)中含NA个中子 |
| B、NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
| C、标准状况下,含有NA个分子的氧气和氮气的混和气体的体积约为22.4L |
| D、制取漂白粉的反应中,每消耗7.1g Cl2,则转移0.2NA个电子 |
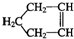 可简写为
可简写为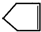 .降冰片烯的分子结构可表示为:
.降冰片烯的分子结构可表示为: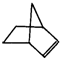
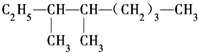 的系统命名法名称是
的系统命名法名称是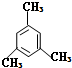 的名称是
的名称是