��Ŀ����
 ��10�֣���֪ij��Һ��ֻ����OH����H+��NH4+��Cl���������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ��
��10�֣���֪ij��Һ��ֻ����OH����H+��NH4+��Cl���������ӣ�ijͬѧ�Ʋ����Һ�и�����Ũ�ȴ�С˳��������������ֹ�ϵ��
A��c(Cl��)��c(NH4+)��c(H+)��c(OH��)
B��c(Cl��)��c(NH4+)��c(OH��)��c(H+)
C��c(Cl��)��c(H+)��c(NH4+)��c(OH��)
D��c(NH4+)��c(Cl��)��c(OH��)��c(H+)
��1������Һ��ֻ�ܽ���һ�����ʣ��������� ����������Ũ�ȴ�С˳���ϵ����ȷ���ǣ�ѡ����ţ� ��
��2����������ϵ��D����ȷ�ģ���Ϻ���Һ�е�����Ϊ ��
��3��25 ��ʱ����a mol��L��1�İ�ˮ��b mol��L��1����������ϣ���Ӧ����Һǡ�������ԣ�����ǰa b���>������<������=����, ��a��b��ʾNH3��H2O�ĵ���ƽ�ⳣ��Ϊ ��
��1��NH4Cl ��A ��2�� NH4Cl NH3��H2O ��3�� > b�� ��mol��L��1
��mol��L��1
��������
����������κ�ˮ��Һ�о�����OH����H+������ȥ��OH����H+��ʣ�µ����Ӿ������ʲ����ģ���ˢ�������Ϊ�Ȼ�李�������Һ�У���ΪNH4+ˮ�⣬����c(Cl��)��c(NH4+)��c(H+)��c(OH��)������ѡA����2��Ҫ��ΪDѡ���Ҫ����c(NH4+)������Ҫ��NH4Cl���ʵĻ����ϼ�NH3��H2O����������ΪNH4Cl��NH3��H2O������3����a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һ�����ԣ���ˮ����������ǰa >b����Һ��c��OH-��=1��10-7mol/L����Һ��c��NH4+��=c��Cl-��= mol/L����Ϻ�Ӧǰc��NH3?H2O��=
mol/L����Ϻ�Ӧǰc��NH3?H2O��= mol/L����Ӧ��c��NH3?H2O��=��
mol/L����Ӧ��c��NH3?H2O��=�� -
- ��mol/L��
��mol/L��
��k=  =
=  =
=  ��10-7��
��10-7��
���㣺��������ˮ�⡣

(8�֣��о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��һ�������£���2molNO��2molO2���ں����ܱ������з�����Ӧ2NO(g)+O2(g) 2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬���� ��
2NO2(g)�����и�����˵����Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ���
b�����������ɫ���ֲ���
c��NO��O2�����ʵ���֮�ȱ��ֲ���
d��ÿ����1 molO2ͬʱ����2 molNO2
��2��CO�����ںϳɼ״���һ���¶��£������Ϊ2L���ܱ������м���CO��H2��������ӦCO��g��+2H2��g�� CH3OH��g������ƽ����ø����Ũ�����£�
CH3OH��g������ƽ����ø����Ũ�����£�
���� | CO | H2 | CH3OH |
Ũ��(mol?L��1) | 0��9 | 1��0 | 0��6 |
����ʽ������ƽ�ⳣ��K=__________________________��
���������¶ȣ�Kֵ������Ӧ�ġ�H 0(�>����<��)��
��������������䣬�ٳ���0��6molCO��0��4molCH3OH,��ʱv��___v��(�>������<����=��)
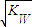 mol��L����1
mol��L����1 2R(g)+2S(s)
2R(g)+2S(s)