题目内容
17.常温下,向pH=2的醋酸溶液中加入少量0.01mol•L-1的盐酸,溶液中一定发生变化的是( )| A. | c(CH3COO-) | B. | KW | C. | Ka(CH3COOH) | D. | c(H+) |
分析 常温下,向pH=2的醋酸溶液中加入少量0.01mol•L-1的盐酸,由于温度不变,则水的离子积、醋酸的电离平衡常数不发生变化;由于溶液体积变化,则溶液中醋酸根离子浓度变化,根据醋酸的电离平衡常数不变可知,溶液中氢离子也一定发生变化,据此进行判断.
解答 解:常温下,向pH=2的醋酸溶液中加入少量0.01mol•L-1的盐酸,由于温度不变,则水的离子积、醋酸的电离平衡常数不发生变化,故B、C错误;
由于加入盐酸中溶液体积会发生变化,则溶液中醋酸根离子的浓度发生变化,而醋酸的电离平衡常数不变,溶液中氢离子也一定发生变化,故A、D正确,
故选AD.
点评 本题考查了弱电解质的电离平衡及其影响,题目难度中等,注意明确水的离子积、电离平衡常数只受温度影响,熟练掌握影响化学平衡的因素.

练习册系列答案
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案
相关题目
7.下列实验过程中,溶液的pH减小的是( )
| A. | 以碳棒为两极电解氢氧化钠溶液 | B. | 向稀盐酸中滴加NaOH溶液 | ||
| C. | 以碳棒为两极电解饱和氯化钠溶液 | D. | 向氢氧化钠溶液中加水 |
8.烧杯中盛有100mL 0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
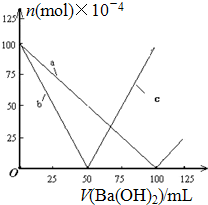

| A. | 曲线a表示Ba2+的物质的量的变化 | |
| B. | 曲线c表示OH-的物质的量的变化 | |
| C. | 加入Ba(OH)2溶液50mL时反应的离子方程式为:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 加入Ba(OH)2溶液大于50mL后,反应的离子方程式为:OH-+H+═H2O |
5.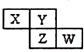 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
 X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )
X、Y、Z均为短周期元素,它们在周期表中相对位置如图所示.若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是( )| A. | Z的离子半径小于Y的离子半径 | |
| B. | W的最高价氧化物对应水化物的酸性比Z的强 | |
| C. | Z的非金属性比Y的强 | |
| D. | X与Y形成的化合物都易溶于水 |
12.高炉冶铁工艺流程如图.在特殊的燃烧器中使氧气和天然气燃烧:
CH4(g)+2O2(g)═CO2(g)+2H2O(g)(放热反应),
催化反应室发生的反应为(不考虑其他平衡的存在):CH4(g)+H2O(g)?CO(g)+3H2(g)(吸热反应);CH4(g)+CO2(g)?2CO(g)+2H2(g)(吸热反应),
下列说法正确的是( )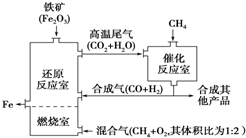
CH4(g)+2O2(g)═CO2(g)+2H2O(g)(放热反应),
催化反应室发生的反应为(不考虑其他平衡的存在):CH4(g)+H2O(g)?CO(g)+3H2(g)(吸热反应);CH4(g)+CO2(g)?2CO(g)+2H2(g)(吸热反应),
下列说法正确的是( )

| A. | 加入铁矿石时,将铁矿石粉碎,目的是加快反应速率提高原料利用率 | |
| B. | 增大催化反应室的压强,甲烷的转化率增大 | |
| C. | 设置燃烧室的目的是产生CO2和水蒸气作原料气与甲烷反应 | |
| D. | 催化反应室需维持在550~750℃,目的仅是提高CH4转化的速率 |
2.实验室用Fe2+的废酸液(pH为1.7)制取氧化铁晶体的流程如图所示.下列说法错误的是( )


| A. | 步骤①中过滤操作需用到的玻璃仪器为玻璃棒、分液漏斗、烧杯 | |
| B. | 步骤②中搅拌操作可加快散热,减少FeCl3水解 | |
| C. | 步骤③中加入的试剂X为浓盐酸 | |
| D. | 步骤⑤中操作a为过滤、洗涤、干燥 |
9.下列叙述错误的是( )
| A. | 用灼烧的方法可以鉴别羊毛和棉花 | |
| B. | 用饱和碳酸钠溶液除去乙酸乙酯中的乙酸 | |
| C. | 用酒精清洗沾到皮肤上的苯酚 | |
| D. | 用酸性高猛酸钾溶液鉴别甲苯和苯乙烯 |
6.下列装置或操作能达到实验目的是( )
| A. | 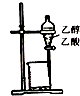 除去乙醇中的乙酸 | B. | 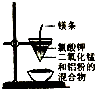 制取少量金属锰 | ||
| C. | 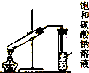 制取乙酸乙酯 | D. | 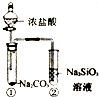 证明酸性:盐酸>碳酸>硅酸 |
7.在标准状况下,在三个干燥的烧瓶内分别装入:纯净的NH3,含有少量空气的NH3,NO2和O2的混合气体[v(NO2):v(O2)=4:1].然后分别做喷泉实验,三个烧瓶中所得溶液的物质的量浓度之比为( )
| A. | 21:12:4 | B. | 5:5:4 | C. | 5:5:1 | D. | 无法确定 |