题目内容
8.烧杯中盛有100mL 0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )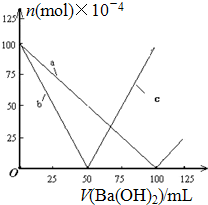
| A. | 曲线a表示Ba2+的物质的量的变化 | |
| B. | 曲线c表示OH-的物质的量的变化 | |
| C. | 加入Ba(OH)2溶液50mL时反应的离子方程式为:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 加入Ba(OH)2溶液大于50mL后,反应的离子方程式为:OH-+H+═H2O |
分析 100mL0.1mol/L的NaHSO4溶液,向其中逐滴滴加0.1mol/L的Ba(OH)2溶液,当氢氧化钡溶液体积小于50mL时,发生反应:2NaHSO4+Ba(OH)2═BaSO4↓+2H2O+Na2SO4,当氢氧化钡溶液体积大于50mL后,硫酸氢钠中氢离子反应完全,再加入氢氧化钡溶液后发生反应:Na2SO4+Ba(OH)2═BaSO4↓+H2O,直至Ba(OH)2溶液过量,硫酸根离子反应完全,据此进行解答.
解答 解:A.由图象曲线变化可知,在加入的氢氧化钡溶液体积小于100mL前,曲线a表示离子的浓度减小,此段曲线a表示的是硫酸根离子,当Ba(OH)2溶液体积大于100mL后,曲线a表示的是钡离子浓度,故A错误;
B.由图可知,曲线c表示离子的浓度先减小后增大,50mLBa(OH)2溶液加入时为0,则直线c表示OH-的物质的量的变化,故B正确;
C.加入Ba(OH)2溶液50mL,反应的化学方程式为:2NaHSO4+Ba(OH)2═BaSO4↓+2H2O+Na2SO4,离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故C错误;
D.加入Ba(OH)2溶液大于50mL后,硫酸氢钠中氢离子已经反应完全,此时的反应为钡离子与硫酸根离子反应生成硫酸钡的反应,反应的离子方程式为:Ba2++SO42-=BaSO4↓,故D错误;
故选B.
点评 本题考查图象与化学反应、离子反应的关系,题目难度中等,明确硫酸氢钠溶液中加入氢氧化钡溶液后发生的反应为解答本题的关键,试题培养了学生的分析、理解能力.

练习册系列答案
相关题目
16.下列除去括号内杂质的有关操作中正确的是( )
| A. | 苯(苯酚) 加浓溴水,振荡,分液 | |
| B. | 福尔马林(甲酸) 加纯碱溶液,分液 | |
| C. | 乙醇(乙酸) 加NaOH溶液,过滤 | |
| D. | 乙酸乙酯(乙酸) 加饱和Na2CO3溶液,分液 |
3.向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )


| A. | 在0~a范围内,只发生中和反应 | |
| B. | ab段发生反应的离子方程式为CO32-+2H+═H2O+CO2 | |
| C. | 原混合溶液中NaOH和Na2CO3的物质的量浓度之比为2:1 | |
| D. | c点对应的溶液中还能大量存在Fe2+、NO3-离子 |
13.下列属于物理变化的是( )
| A. | 煤的干馏 | B. | 钢铁生锈 | C. | 干冰升华 | D. | 食物腐败 |
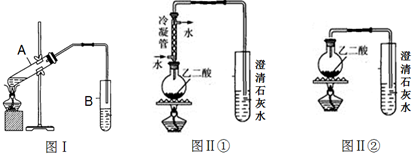
20.下列实验装罝、操作或现象描述正确的是( )
| A. | 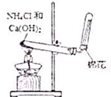 实验室制取NH3 | B. | 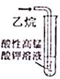 溶液颜色褪去 | C. | 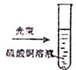 看到光亮的通路 | D. | 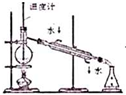 石油蒸馏 |
17.常温下,向pH=2的醋酸溶液中加入少量0.01mol•L-1的盐酸,溶液中一定发生变化的是( )
| A. | c(CH3COO-) | B. | KW | C. | Ka(CH3COOH) | D. | c(H+) |
18.以下化学用语正确的是 ( )
| A. | Cr最外层电子排布式 4s2 | B. | 乙醇的结构简式CH3CH2OH | ||
| C. | 二氧化硅的分子式 SiO2 | D. | 甲醛的电子式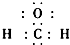 |
 .
.