题目内容
下列离子方程式书写不正确的是( )
| A、将金属Na投入水中:2Na+2H2O=2Na++2OH-+H2↑ |
| B、在硫酸溶液中加入氢氧化钡溶液至中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| C、氯化铁溶液与铁反应:2Fe3++Fe=3Fe2+ |
| D、碳酸钙中滴加盐酸:CO32-+2H+=CO2↑+H2O |
考点:离子方程式的书写
专题:
分析:A.钠与水反应生成氢氧化钠和氢气;
B.浓硫酸与氢氧化钡反应生成硫酸钡和水;
C.氯化铁与铁反应生成氯化亚铁;
D.碳酸钙为沉淀,应保留化学式.
B.浓硫酸与氢氧化钡反应生成硫酸钡和水;
C.氯化铁与铁反应生成氯化亚铁;
D.碳酸钙为沉淀,应保留化学式.
解答:
解:A.将金属Na投入水中,反应生成氢氧化钠和氢气:2Na+2H2O=2Na++2OH-+H2↑,故A正确;
B.浓硫酸与氢氧化钡反应生成硫酸钡和水,离子方程式:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B正确;
C.氯化铁溶液与铁反应生成氯化亚铁,离子方程式:2Fe3++Fe=3Fe2+,故C正确;
D.碳酸钙中滴加盐酸,离子方程式:CaCO3+2H+=CO2↑+H2O+Ca2+,故D错误;
故选:D.
B.浓硫酸与氢氧化钡反应生成硫酸钡和水,离子方程式:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B正确;
C.氯化铁溶液与铁反应生成氯化亚铁,离子方程式:2Fe3++Fe=3Fe2+,故C正确;
D.碳酸钙中滴加盐酸,离子方程式:CaCO3+2H+=CO2↑+H2O+Ca2+,故D错误;
故选:D.
点评:本题考查了离子方程式的书写,明确发生的化学反应是解题关键,注意化学式的拆分.

练习册系列答案
相关题目
有关原电池的下列说法中正确的是( )
| A、在外电路中电子由正极流向负极 |
| B、在原电池中,只有金属锌作为负极 |
| C、原电池工作时,阳离子向正极方向移动 |
| D、原电池工作时,阳离子向负极方向移动 |
标准状况下2.24LCO气体在足量氧气中燃烧后,加足量的过氧化钠充分吸收气体后,过氧化钠质量增加了( )
| A、2.8g | B、4.4g |
| C、10.6g | D、1.4g |
下列离子方程式正确的是( )
| A、FeCl3溶液与Cu的反应:Cu+Fe3+=Cu2++Fe2+ | ||||
| B、NO2与水的反应:3NO2+H2O=2NO3-+2H++NO | ||||
| C、醋酸溶液与水垢中的CaCO3反应:CaCO3+2H+=Ca2++H2O+CO2↑ | ||||
D、用铂电极电解氯化镁溶液:2Cl-+2H2O
|
下列反应的离子方程式正确的是( )
| A、铜与硫酸亚铁反应 Cu+Fe2+═Cu2++Fe |
| B、澄清的石灰水跟盐酸反应 H++OH-═H2O |
| C、碳酸钡溶于醋酸BaCO3+2H+═Ba2++H2O+CO2↑ |
| D、金属钠跟水反应Na+H2O═Na++OH-+H2↑ |
反应A(g)+3B(g)═2C(g)+2D(g)在四种不同情况下的反应速率分别为:
①v(A)=0.45mol/(L?s) ②v(B)=0.6mol/(L?s)
③v(C)=0.4mol/(L?s) ④v(D)=0.45mol/(L?s)
下列有关反应速率的比较中正确的是( )
①v(A)=0.45mol/(L?s) ②v(B)=0.6mol/(L?s)
③v(C)=0.4mol/(L?s) ④v(D)=0.45mol/(L?s)
下列有关反应速率的比较中正确的是( )
| A、④>③=②>① |
| B、④<③=②<① |
| C、①>②>③>④ |
| D、④>③>②>① |
 某课外兴趣小组预测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组预测定某NaOH溶液的浓度,其操作步骤如下:
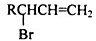
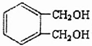 的同分异构体中同时符合下列条件的芳香族化合物共有
的同分异构体中同时符合下列条件的芳香族化合物共有