题目内容
4.以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )| 氧化物 | 环境问题 | 主要来源 | |
| A | CO2 | 酸雨 | 化石燃料的燃烧 |
| B | CO | CO中毒 | 汽车尾气和化石燃料的不完全燃烧 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二氧化硫与酸雨有关,温室效应的罪魁祸首是二氧化碳;
B.一氧化氮为有毒气体;
C.二氧化氮与光化学烟雾有关,与温室效应;
D.二氧化硫与酸雨有关,光化学烟雾与二氧化氮有关.
解答 解:A.化石燃料燃烧主要排放二氧化碳气体,与温室效应有关,而与酸雨无关,故A错误;
B.汽车尾气和化石燃料的不完全燃烧会产生CO,CO为有毒气体,故B正确;
C.温室效应的罪魁祸首为二氧化碳,不是二氧化氮,故C错误;
D.二氧化硫是形成酸雨的主要污染物,而光化学烟雾与二氧化氮有关,且汽车尾气的排放的主要为C、N的氧化物,故D错误;
故选B.
点评 本题考查常见的生活环境的污染治理,题目难度不大,注意掌握污染物的形成条件及防治方法,试题侧重基础知识的考查,培养了学生的环境保护意识.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.恒温、恒压下,在一个容积可变的容器中发生如下反应:N2+3H2?2NH3
(1)若开始时放入1mol N2和3mol H2,达到平衡后,生成a mol NH3
(2)若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3a mol,则开始时放入N2和H2的物质的量分别为( )
(1)若开始时放入1mol N2和3mol H2,达到平衡后,生成a mol NH3
(2)若开始时无NH3,只放入N2和H2,达到平衡时生成NH3的物质的量为3a mol,则开始时放入N2和H2的物质的量分别为( )
| A. | 1mol和9mol | B. | 2mol和9mol | C. | 3mol和9mol | D. | 3mol和6mol |
12.设 NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 在反应 KClO3+6HCl═KCl+3Cl2↑+3H2O 中,Cl2既是氧化产物又是还原产物,当得到标准状况下的 67.2 L Cl2 时,反应中转移的电子数为 5NA | |
| B. | 标准状况下,22.4 L 甲苯中含有的 C-H 键数目为 8NA | |
| C. | 50 g 46%的乙醇水溶液中,含氢原子总数目为 3NA | |
| D. | t℃时,MgCO3的 Ksp=4×10-6,则该温度下饱和 MgCO3溶液中含有的 Mg2+数目为 2×10-3 NA |
9.下列说法不正确的是( )
| A. | “光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关 | |
| B. | Al(OH)3可作阻燃剂,因此可以用于灭火 | |
| C. | SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱 | |
| D. | 焰火的五彩缤纷是某些金属元素的性质的展现 |
16.下列溶液中物质的量浓度为1mol•L-1的是( )
| A. | 将40g NaOH溶解于1L水中 | |
| B. | 将22.4L氯化氢气体溶于水配成1L溶液 | |
| C. | 从100mL 10mol•L-1的浓盐酸中取出10mL | |
| D. | 20g NaOH溶解在水中配成500mL溶液 |
14.已知硅酸盐中,通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式.Si2O44-四面体可用图(a)表示.图(b)是一种无限长单链结构的多硅酸根,其化学式为( )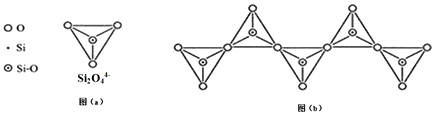

| A. | Si2O76- | B. | Si2O52- | C. | SiO32- | D. | Si4O116- |

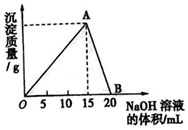 向20ml某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示:
向20ml某浓度的AlCl3溶液中滴加2mol/L的NaOH溶液时,所得的沉淀质量与加入NaOH溶液的体积之间的关系如图所示: