题目内容
6.在一定条件下,常温常压下的水可瞬间结成冰,俗称“热冰”,下列说法正确的是( )| A. | “热冰”与水的化学性质相同 | B. | “热冰”在任何条件下都不会融化 | ||
| C. | 水结成“热冰”分子间的间隔变大 | D. | 结成“热冰”后,分子停止运动 |
分析 只要抓住热冰是有水凝结而成的,也就是热冰的实质还是水,物质发生三态变化时物质本身并无变化,只是分子间隔发生了改变,属物理变化.
解答 解:A.热冰与水同属一种物质,物理性质不同,化学性质相同,故A正确;
B.物质都有三态变化,热冰也不例外,故B错误;
C.水结成“热冰”分子间的间隔变小,故C错误;
D.分子永远不停的运动,热冰也不例外,故D错误.
故选:A.
点评 本题考查物质状态的变化,此题是对物质的三态变化进行的探讨,涉及到物质三态变化的实质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.用NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 常温常压下,2.24LO2、O3的混合气体含有NA个分子 | |
| B. | 28 g CO和N2混合气体含有NA个分子 | |
| C. | 标准状况下,4.48 L水含有的分子数等于0.2NA | |
| D. | 标准状况下,CO2与Na2O2反应生成2.24 L O2转移的电子数为0.4NA |
7.设NA为阿伏加德罗常数的值.下列有关叙述正确的是( )
| A. | 25℃时,1LpH=11的氨水中OH-为0.001NA | |
| B. | 标准状况下,2.24LSO3的氧原子数为0.3NA | |
| C. | 4.6g乙醇中含有的共价键数为0.7NA | |
| D. | 3.6gD2O所含质子数为2NA |
1.室温时,将V mL硫酸铜不饱和溶液蒸发a克水后析出b克CuSO4•5H2O晶体,剩余溶液再蒸发2a克水恰好全部变成c克CuSO4•5H2O晶体,则下列叙述正确的是( )
| A. | 原溶液中含有硫酸铜$\frac{4}{5}$(b+C)g | |
| B. | 原溶液浓度为 $\frac{4(b+C)}{V}$mol/L | |
| C. | 室温时硫酸铜溶解度为$\frac{160C}{50a+9C}$g | |
| D. | 原溶液的溶质质量分数为$\frac{32(b+C)}{3a+b+C}$% |
11.下列事故处理不正确的是 ( )
| A. | 不慎碰倒酒精灯,洒出的酒精在桌上燃烧时,应立即用湿抹布扑盖 | |
| B. | 将一氧化碳中毒者移到通风处抢救 | |
| C. | 实验室中金属钠不慎着火后,立马使用细沙盖灭 | |
| D. | 不慎将浓硫酸溅到皮肤上,应立即用水冲洗 |
18.原子序数依次增大的A、B、C、D、E五种短周期元素.A、B可形成密度为0.76g/L(标准状况下) 的气体,C的最外层电子数为其内层电子数的3倍,A与D、C与E同主族.下列说法正确的是( )
| A. | D2E2和A2C2两种化合物对应晶体中的化学键类型相同 | |
| B. | 只含A、B、C三种元素的某化合物水溶液,可能呈碱性或酸性 | |
| C. | 原子半径大小:D>B>C;简单离子半径大小:D+>E2->C2- | |
| D. | A2C的稳定性强于A2E、沸点高于A2E,均因为A-C键键能大于A-E键键能 |
16.下列说法正确的是( )
| A. | 氧化铜的摩尔质量是80 g | B. | 氨气的摩尔质量是17 mol | ||
| C. | 氧气的摩尔质量是32 g•mol-1 | D. | 1 mol氢原子的质量是2 g |
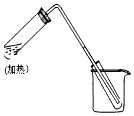 如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置(加热及固定仪器略),其原理与教材中的实验完全相同.回答下列问题: