题目内容
关于常温下0.1mol/L氨水(pH=11.12)的下列说法不正确的是( )
| A、加水稀释过程中,c(H+):c(OH-) 的值增大 | ||
| B、根据以上信息,可推断NH3?H2O为弱电解质 | ||
C、与pH=11.12的 NaOH溶液相比,NaOH溶液中c(Na+) 大于氨水中c(NH
| ||
| D、加入少量NH4Cl 固体,溶液中水的电离平衡:H2O?H++OH-正向移动 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:A、加水稀释过程中,促进电离,但显性离子氢氧根离子浓度减小,而温度不变水的离子积常数不变,所以氢离子浓度增大;
B、如果是强电解质,0.1mol/L氨水的pH=13;
C、根据两溶液中电荷守恒分析解答;
D、NH4Cl 是强酸弱碱盐,溶于水要发生水解,盐的水解对水的电离起促进作用.
B、如果是强电解质,0.1mol/L氨水的pH=13;
C、根据两溶液中电荷守恒分析解答;
D、NH4Cl 是强酸弱碱盐,溶于水要发生水解,盐的水解对水的电离起促进作用.
解答:
解:A、加水稀释过程中,促进电离,但显性离子氢氧根离子浓度减小,而温度不变水的离子积常数不变,所以氢离子浓度增大,所以c(H+):c(OH-) 的值增大,故A正确;
B、如果是强电解质,0.1mol/L氨水的pH=13,故B正确;
C、氢氧化钠溶液中c(Na+)+c(H+)=c(OH-),在氨水溶液中c(NH4+)+c(H+)=c(OH-),而两者的PH相同,所以两溶液中氢离子与氢氧根离子浓度相等,则钠离子与铵根离子浓度相等,故C错误;
D、水的电离平衡:H2O?H++OH-,铵根离子结合水电离出的氢氧根离子,导致氢氧根离子浓度减小,所以平衡正向移动,故D正确;
故选C.
B、如果是强电解质,0.1mol/L氨水的pH=13,故B正确;
C、氢氧化钠溶液中c(Na+)+c(H+)=c(OH-),在氨水溶液中c(NH4+)+c(H+)=c(OH-),而两者的PH相同,所以两溶液中氢离子与氢氧根离子浓度相等,则钠离子与铵根离子浓度相等,故C错误;
D、水的电离平衡:H2O?H++OH-,铵根离子结合水电离出的氢氧根离子,导致氢氧根离子浓度减小,所以平衡正向移动,故D正确;
故选C.
点评:本题考查了弱电解质的电离和盐的水解,明确弱电解质电离特点是解本题关键,注意电荷守恒在解题中的应用,题目难度不大.

练习册系列答案
相关题目
向13.6gCu和Cu2O的混合物中加入某浓度的稀硝酸0.25L,固体物质完全反应,生成NO和Cu(NO3)2.在所得溶液中加入0.5mol/L的NaOH溶液1L,反应后溶液恰好呈中性,金属离子已完全沉淀,沉淀质量为19.6g,下列说法不正确的是( )
| A、Cu与Cu2O的物质的量之比为2:1 |
| B、硝酸的物质的量浓度为2 mol/L |
| C、Cu、Cu2O与硝酸反应后剩余HNO3的物质的量为0.5mol |
| D、产生的NO在标准状况下的体积为2.24L |
下列实验正确的是( )
A、 蒸发、浓缩、结晶 |
B、 检查装置气密性 |
C、 碳酸氢钠受热分解 |
D、 分离沸点不同且互溶的液体混合物 |
将2.3g钠放入100g水中,生成溶液中溶质的质量分数是( )
| A、等于2.3% | B、小于4% |
| C、等于4% | D、大于4% |
下列说法正确的是( )
| A、硅材料广泛用于光纤通讯 |
| B、工艺师利用盐酸刻蚀石英制作艺术品 |
| C、粗硅制备单晶硅不涉及氧化还原反应 |
| D、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
化学在生产和生活中有重要的应用.下列说法不正确的是( )
| A、电解MgCl2溶液可制金属镁 |
| B、可溶性铁盐或铝盐可用于水的净化 |
| C、在海轮外壳上装上锌块,可减缓船体的腐蚀速率 |
| D、“开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |
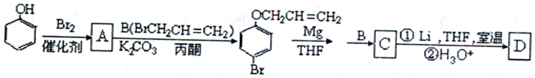
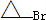 是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有
是化合物B的一种同分异构体,用核磁共振氢谱可以证明该化合物中有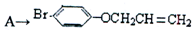 的有机反应类型
的有机反应类型