题目内容
下列操作中最终没有沉淀析出的是( )
| A、向饱和Na2CO3(aq)中通入过量的CO2 |
| B、向饱和的食盐水中加入一小块间质钠 |
| C、向CaCl2(aq)中通入少量的CO2气体 |
| D、向AlCl3(aq)滴入过量稀氨水 |
考点:钠的重要化合物,镁、铝的重要化合物
专题:元素及其化合物
分析:A.过量CO2和Na2CO3反应生成NaHCO3,Na2CO3的溶解性大于NaHCO3,所以溶液为过饱和溶液;
B.向饱和的食盐水中加入一小块间质钠,钠与水反应生成氢氧化钠和氢气,消耗水,则溶液为过饱和溶液;
C.H2CO3酸性小于盐酸,所以CaCl2溶液和CO2不反应;
D.因为氢氧化铝只与强酸强碱反应,所以向AlCl3(aq)滴入过量稀氨水生成氢氧化铝和氯化铵.
B.向饱和的食盐水中加入一小块间质钠,钠与水反应生成氢氧化钠和氢气,消耗水,则溶液为过饱和溶液;
C.H2CO3酸性小于盐酸,所以CaCl2溶液和CO2不反应;
D.因为氢氧化铝只与强酸强碱反应,所以向AlCl3(aq)滴入过量稀氨水生成氢氧化铝和氯化铵.
解答:
解:A.过量CO2和Na2CO3反应生成NaHCO3,Na2CO3的溶解性大于NaHCO3,所以溶液为过饱和溶液,则有NaHCO3晶体析出,故A正确;
B.向饱和的食盐水中加入一小块间质钠,钠与水反应生成氢氧化钠和氢气,消耗水,则溶液为过饱和溶液,所以有NaCl晶体析出,故B正确;
C.H2CO3酸性小于盐酸,所以CaCl2溶液和CO2不反应,所以最终没有沉淀析出,故C错误;
H2CO3酸性大于HClO,Ca(ClO)2溶液和CO2反应生成CaCO3和HClO,但过量的CO2和CaCO3反应生成可溶性的Ca(HCO3)2,所以最终没有沉淀析出,故C错误;
D.因为氢氧化铝只与强酸强碱反应,所以向AlCl3(aq)滴入过量稀氨水生成氢氧化铝沉淀和氯化铵,故D正确;
故选C.
B.向饱和的食盐水中加入一小块间质钠,钠与水反应生成氢氧化钠和氢气,消耗水,则溶液为过饱和溶液,所以有NaCl晶体析出,故B正确;
C.H2CO3酸性小于盐酸,所以CaCl2溶液和CO2不反应,所以最终没有沉淀析出,故C错误;
H2CO3酸性大于HClO,Ca(ClO)2溶液和CO2反应生成CaCO3和HClO,但过量的CO2和CaCO3反应生成可溶性的Ca(HCO3)2,所以最终没有沉淀析出,故C错误;
D.因为氢氧化铝只与强酸强碱反应,所以向AlCl3(aq)滴入过量稀氨水生成氢氧化铝沉淀和氯化铵,故D正确;
故选C.
点评:本题考查物质之间的反应,明确物质的性质及物质的溶解性即可解答,易错选项是A,注意Na2CO3、NaHCO3溶解性相对大小,为易错点.

练习册系列答案
相关题目
下列说法正确的是( )
| A、某钾盐溶于盐酸,产生无色无味的气体,将气体通入澄清石灰水,有白色沉淀生成,则该钾盐一定是K2CO3 |
| B、取试剂少量于试管,滴加入少量BaCl2溶液,生成白色沉淀,加稀HNO3白色沉淀不溶解,证明该试剂中一定含SO42- |
| C、用某盐做焰色反应,火焰为黄色,说明该盐一定含Na+,一定不含K+ |
| D、取黄色溶液少量于试管,滴加KSCN(aq),呈红色,该溶液中一定含有Fe3+ |
某溶液由相同物质的量的CuCl2、FeCl3、AlCl3混合而成,向该溶液中加入铁粉,充分搅拌后振荡,铁粉仍有剩余,则溶液中存在较多的阳离子是( )
| A、Fe2+、Al3+ |
| B、Fe2+、Fe3+ |
| C、Fe3+、Al3+ |
| D、Fe2+、Cu2+ |
过量的下列溶液与水杨酸 反应能得到化学式为C7H5O3Na的是( )
反应能得到化学式为C7H5O3Na的是( )
 反应能得到化学式为C7H5O3Na的是( )
反应能得到化学式为C7H5O3Na的是( )| A、NaHCO3溶液 |
| B、Na2CO3溶液 |
| C、NaOH溶液 |
| D、NaCl溶液 |
利用下列装置进行相应实验,不能达到实验目的是( )

| A、图①装置可验证酸性:H2CO3>H2SiO3 |
| B、图②装置可用于收集气体H2、CO2、Cl2、NH3 |
| C、图③装置可用于分离互不相溶的两种液体 |
| D、图④装置可制备Fe(OH)2并能较长时间保持其颜色 |
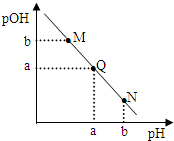 某温度下,向一定体积的0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的关系如图[已知:pOH=-lgc(OH-)],下列说法正确的是
某温度下,向一定体积的0.1mol/L的醋酸溶液中逐滴加入等浓度的NaOH溶液,溶液中pOH与pH的关系如图[已知:pOH=-lgc(OH-)],下列说法正确的是( )
| A、M点溶液导电能力强于Q点溶液导电能力 |
| B、N点所示溶液中,c(CH3COO-)>c(Na+) |
| C、M点与N点所示溶液中水的电离程度相等 |
| D、Q点消耗NaOH溶液体积等于醋酸溶液的体积 |
化学与社会、生活密切相关,下列说法正确的是( )
| A、“歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 |
| B、工业上通常用电解Na、Mg、Al对应的氯化物制取该三种金属单质 |
| C、Fe3O4俗称铁红,常做红色油漆和涂料 |
| D、燃料电池的燃料都在负极发生氧化反应 |

