题目内容
下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 用激光笔照射鸡蛋清水溶液 | 有丁达尔效应 | 鸡蛋清分子直径介于1nm~100nm |
| B | 向某氯化亚铁溶液中滴入少量氯水,然后滴入少量的KSCN溶液 | 溶液变成血红色 | 说明原氯化亚铁已氧化变质 |
| C | 加热分解某盐X,将产生的气体通入硝酸酸化的BaCl2溶液 | 实验开始立即产生白色沉淀 | X可能是NaHCO3 |
| D | 向溶液X中滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价,物质的检验和鉴别的实验方案设计
专题:实验评价题
分析:A.丁达尔现象为胶体特有的性质;
B.向某氯化亚铁溶液中滴入少量氯水,氯气可氧化亚铁离子;
C.二氧化碳与硝酸酸化的BaCl2溶液不反应;
D.滴加稀NaOH溶液,不能生成氨气.
B.向某氯化亚铁溶液中滴入少量氯水,氯气可氧化亚铁离子;
C.二氧化碳与硝酸酸化的BaCl2溶液不反应;
D.滴加稀NaOH溶液,不能生成氨气.
解答:
解:A.丁达尔现象为胶体特有的性质,由现象可知,鸡蛋清水溶液为胶体分散系,则鸡蛋清分子直径介于1nm~100nm,故A正确;
B.向某氯化亚铁溶液中滴入少量氯水,氯气可氧化亚铁离子,不能检验是否变质,应先加KSCN溶液、再加氯水检验,故B错误;
C.二氧化碳与硝酸酸化的BaCl2溶液不反应,则由现象可知,白色沉淀为硫酸钡,则X可能是NaHSO3,故C错误;
D.滴加稀NaOH溶液,不能生成氨气,应加浓NaOH、加热后用湿润红色石蕊试纸检验气体,确定是否含铵根离子,故D错误;
故选A.
B.向某氯化亚铁溶液中滴入少量氯水,氯气可氧化亚铁离子,不能检验是否变质,应先加KSCN溶液、再加氯水检验,故B错误;
C.二氧化碳与硝酸酸化的BaCl2溶液不反应,则由现象可知,白色沉淀为硫酸钡,则X可能是NaHSO3,故C错误;
D.滴加稀NaOH溶液,不能生成氨气,应加浓NaOH、加热后用湿润红色石蕊试纸检验气体,确定是否含铵根离子,故D错误;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及离子的检验、胶体的性质及氧化还原反应等,把握反应原理及反应与现象的关系为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
下列有关实验操作不正确的是( )
| A、给盛有液体的烧瓶加热时,需要加碎瓷片或沸石 |
| B、CCl4萃取碘水中碘的实验,分液时,水层应从分液漏斗下口放出,CCl4层从应上口倒出 |
| C、用容量瓶配制溶液,定容时加水超过了刻度线,必须进行重新配制 |
| D、测定溶液pH时,应用干燥洁净的玻璃棒蘸取溶液点在pH试纸上跟标准比色卡对照 |
下列生产工艺措施合理的是( )
| A、用SO2漂白银耳 |
| B、用硫酸清洗锅炉中的水垢 |
| C、高温下用镁还原SiO2制取粗硅 |
| D、用Na2S作沉淀剂,除去废水中Cu2+和Hg2+ |
下列说法正确的是( )
| A、100ml1mol/LAlCl3溶液中含的阳离子数为0.1NA |
| B、含1 mol H2SO4的浓硫酸与足量铜反应转移的电子总数为6.02×1023 |
| C、同温同压下,1 L CO和H2的混合气体完全燃烧消耗0.5 L O2 |
| D、相同物质的量OH-和CH3+含有相同数目的电子 |
下列有关叙述正确的是( )
| A、明矾在水中生成的Al(OH)3胶体有吸附性,因此常用明矾对水进行净化和消毒 |
| B、二氧化硅具有较强的导电性,可用于制造光导纤维 |
| C、CO2、SO2、NO2都能和碱溶液发生反应,因此它们都属于酸性氧化物 |
| D、常温下干燥的氯气不与铁反应,所以可以用钢瓶贮存液氯 |
下列装置图正确的是( )
A、 容量瓶定容 |
B、 海水蒸馏原理 |
C、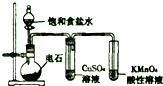 验证乙炔的性质 |
D、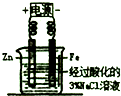 验证牺牲阳极的阴极保护法 |
下列各组物质中,按单质、化合物、混合物顺序排序正确的是( )
| A、石墨、大理石、胆矾 |
| B、铁矿、小苏打、空气 |
| C、水银、水蒸气、氯水 |
| D、金属钠、食盐水、双氧水 |
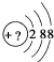 (1)该微粒是中性微粒,这种微粒的符号是
(1)该微粒是中性微粒,这种微粒的符号是