题目内容
8.表为元素周期表的一部分,请用化学用语回答有关问题:| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ⑨ | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)元素⑥形成的氢化物的电子式是
 ;
;(3)表中能形成两性氢氧化物的元素是Al(填写元素符号),请写出该元素的氢氧化物与⑨最高价氧化物对应的水化物发生反应的化学方程式Al(OH)3+NaOH=NaAlO2+2H2O.
分析 根据元素在周期表中的位置可知,①②③④⑤⑥⑦⑧⑨分别是N、F、Mg、Al、Si、S、Cl、Ar、Na元素.
(1)由①和⑧的位置可知;
(2)S元素的氢化物为硫化氢,通过共用电子对形成共价化合物;
(3)铝能形成两性氢氧化物,氢氧化铝与氢氧化钠反应生成盐和水.
解答 解:(1)由①和⑧的位置可知两种元素分别是N和Ar,
故答案为:N;Ar;
(2)S元素的氢化物为H2S,H2S是共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H-S键,电子式为: ,
,
故答案为: ;
;
(3)铝能形成两性氢氧化物,氢氧化铝与氢氧化钠反应生成偏铝酸钠与水,反应的化学方程式为Al(OH)3+NaOH=NaAlO2+2H2O,
故答案为:Al;Al(OH)3+NaOH=NaAlO2+2H2O.
点评 本题考查位置、结构、性质的关系,为高频考点,把握元素的位置推断元素及元素化合物知识为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
18.同一物质在化学反应中断键需要吸热,成键需要放热且数值相等.物质含有的能量越高越不稳定,含有的能量越低越稳定.表中的数据是破坏1mol物质中的化学键所消耗的能量:
根据上述数据回答下列问题:
(1)下列物质本身具有的能量最低的是A.
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中最稳定的是A.A.HClB.HBrC.HI
(3)Cl2+H2=2HCl 的反应是B反应.A.吸热反应B.放热反应.
| 物质 | Cl2 | Br2 | I2 | HCl | HBr | HI | H2 |
| 能量(kJ) | 243 | 193 | 151 | 431 | 366 | 298 | 436 |
(1)下列物质本身具有的能量最低的是A.
A.H2 B.Cl2 C.Br2 D.I2
(2)下列氢化物中最稳定的是A.A.HClB.HBrC.HI
(3)Cl2+H2=2HCl 的反应是B反应.A.吸热反应B.放热反应.
19.改变了“有机物就是有生命力的物质”观点的科学家是( )
| A. | 李比希 | B. | 维勒 | C. | 凯库勒 | D. | 诺贝尔 |
3.下列反应过程中的能量变化情况符合如图的是( )
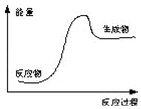

| A. | 石灰石高温分解反应 | B. | 镁和盐酸的反应 | ||
| C. | 酸与碱的中和反应 | D. | 氧化钙和水的反应 |
13.用括号中的试剂除去各组物质中的杂质,可选试剂不正确的是( )
| A. | 乙醇中的水(新制CaO) | B. | 乙烷中乙烯(溴水) | ||
| C. | 苯中的甲苯(溴水) | D. | 乙酸乙酯中的乙酸(饱和Na2CO3溶液) |
20.表是元素周期表的一部分,回答下列有关问题:
(1)写出元素符号:⑨Ar(填化学式,下同)
(2)在这些元素中,最活泼的金属元素是K.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
(2)在这些元素中,最活泼的金属元素是K.
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是HClO4,呈两性的氢氧化物是Al(OH)3.
17.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:
①取少量样品加入足量水溶解;再加入足量氢氧化钠溶液(微热),产生白色沉淀并有气泡冒出.
②取少量样品加入足量稀盐酸有气泡产生,振荡后固体完全溶解.
该白色粉末可能为( )
①取少量样品加入足量水溶解;再加入足量氢氧化钠溶液(微热),产生白色沉淀并有气泡冒出.
②取少量样品加入足量稀盐酸有气泡产生,振荡后固体完全溶解.
该白色粉末可能为( )
| A. | NaHCO3、MgCl2 | B. | NH4HCO3、AlCl3 | C. | (NH4)2 CO3、BaCl2 | D. | NH4 HCO3、MgCl2 |
18.下列叙述中,正确的是( )
| A. | 某物质中只含有一种元素,该物质一定是纯净物 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | 含有离子键的化合物一定是离子化合物 | |
| D. | 离子化合物只含离子键 |