题目内容
6.a、b、c、d均为短周期元素,a的原子中只有1个电子,b2-和c+离子的电子层结构相同,b与d同主族.下列叙述正确的是( )| A. | a分别与b、c、d形成的二元化合物中a的化合价均为+1 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | a与b形成的化合物中一定只有共价键,b与c形成的化合物中一定只有离子键 | |
| D. | 原子半径大小顺序d>c>b>a |
分析 a、b、c、d为短周期元素,a的原子中只有1个电子,则a为H元素;b2-和c+的电子层结构相同,结合离子所得电荷可知b为O元素,c为Na元素;d与b同族,则d为S元素,结合元素化合物性质与元素周期律解答.
解答 解:a、b、c、d为短周期元素,a的原子中只有1个电子,则a为H元素;b2-和c+的电子层结构相同,结合离子所得电荷可知b为O元素,c为Na;d与b同族,则d为S元素,
A.H元素与Na形成化合物NaH,H元素为-1价,故A错误;
B.O元素与H元素形成H2O、H2O2,与Na元素形成Na2O、Na2O2,与S元素形成SO2、SO3,故B正确;
C.H与O元素形成的水和双氧水只含有共价键,而O与Na形成的过氧化钠中含有共价键,故C错误;
D.电子层越多,原子半径越大,电子层相同时,核电荷数越大,原子半径越小,则原子半径大小为:c>d>b>a,故D错误;
故选B.
点评 本题考查结构性质位置关系应用,注意抓住短周期推断元素,熟练掌握元素化合物知识,注意对元素周期律的理解掌握,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
16.含SO2的工业尾气可用石灰乳吸收处理,再经氧化制得CaSO4•2H2O(石膏),若处理含SO2 0.224%(体积分数)的尾气1×106 m3(标准状况),假定原料利用率均为100%,理论上可得到石膏的质量为(吨)( )
| A. | 17.2 | B. | 1.72 | C. | 1.2 | D. | 0.0172 |
17.下列气体中,只能用排水法收集的是( )
| A. | NO | B. | NO2 | C. | CO2 | D. | H2 |
18.一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料电池的说法正确的是( )
| A. | 在熔融电解质中,O2-由正极移向负极 | |
| B. | 当负极消耗4.48L气体时,转移电子5.2mole- | |
| C. | 电子的流动方向:负极经外电路流向正极,再通过内电路流回负极 | |
| D. | 通入丁烷的一极是负极,电极反应为:C4H10-26e-+13O2-═4CO2+5H2O |
6.下列有机化合物的命名正确的是( )
| A. |  :二溴乙烷 :二溴乙烷 | B. |  :1-甲基-1-丙醇 :1-甲基-1-丙醇 | ||
| C. | 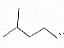 :4-甲基戊烷 :4-甲基戊烷 | D. | 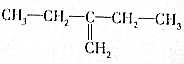 :2-乙基-1-丁烯 :2-乙基-1-丁烯 |
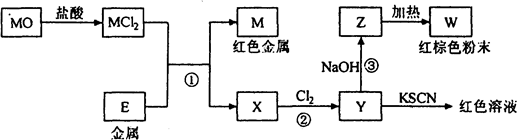
 如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题:
如图是一个甲烷燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时,M、N两个电极的质量都不减少,请回答下列问题: ④
④ 等,其中C原子为sp2杂化的分子有①③④(填序号),预测HCHO分子的立体结构为平面三角形.
等,其中C原子为sp2杂化的分子有①③④(填序号),预测HCHO分子的立体结构为平面三角形.