题目内容
15.某化学反应的能量变化如图所示.下列有关叙述正确的是( )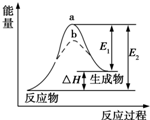
| A. | 如图可知a一定使用了催化剂 | |
| B. | 该反应为放热反应,△H=E1-E2 | |
| C. | 使用催化剂,可以改变化学平衡常数 | |
| D. | 使用催化剂,可降低该反应的活化能 |
分析 A.加入催化剂会降低反应的活化能;
B.根据图象分析可知反应物能量低于生成物能量,为吸热反应;
C.加入催化剂不会改变化学反应平衡;
D.催化剂能降低反应的活化能,从而加快化学反应速率;
解答 解:A.催化剂会降低反应的活化能,a、b分别对应无催化剂和有催化剂的能量变化,故A错误;
B.焓变△H=E2-E1,反应为吸热反应,故B错误;
C.加入催化剂不会改变化学反应的平衡,化学平衡常数不变,故C错误.
D.催化剂能降低反应的活化能,从而加快化学反应速率,故D正确;
故选D.
点评 本题考查了反应能量变化的分析判断,图象分析是解题关键,反应的能量守恒是判断的依据,注意加入催化剂不会改变化学平衡,会降低反应的活化能,题目较简单.

练习册系列答案
相关题目
5.如图所示的实验操作中,正确的是( )
| A. | 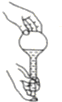 检查容量瓶是否漏水 | B. | 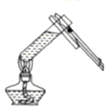 给液体加热 | ||
| C. |  滴加液体 | D. | 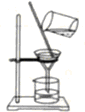 过滤 |
6.已知4NH3(g)+5O2(g)═4NO(g)+6H2O(g),若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则下列关系正确的是( )
| A. | 4 v(NH3)=5 v(O2) | B. | 5v(O2)=6 v(H2O) | C. | 2 v(NH3)=3 v(H2O) | D. | 4v(O2)=5 v(NO) |
3.巴黎气候大会揭开了发展低碳经济的宏伟序幕,下列有关说法正确的是( )


| A. | 太阳能、地热能、核能、化石燃料等均属于“新能源” | |
| B. | 减少含碳物质做燃料符合“低碳”理念 | |
| C. | 图中转化途径不能体现“节能减排”的思想 | |
| D. | 节约用电不能减少CO2的排放量 |
20.在101kPa时,1mol纯物质完全燃烧生成稳定的氧化物时所放出的热量,叫做该物质的燃烧热,甲烷的燃烧热是890.3kJ•mol-1,则下列热化学方程式书写正确的是( )
| A. | CH4(g)+$\frac{3}{2}$O2(g)═CO(g)+2H2O(l)△H=-890.3kJ•mol-1 | |
| B. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3kJ•mol-1 | |
| D. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3kJ•mol-1 |
7.某化学兴趣小组设计如下方案测定饱和食盐水的电解率.
[提示:饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%]
方案一:连接图甲、乙装置,在洗气瓶a中盛放足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率.

(1)正确的连接顺序为导管口B(填“A”或“B”)连导管口C,若事先往甲装置的饱和食盐水中滴入酚酞,则电解过程甲装置中铁棒(填“铁棒”或“碳棒”)附近的溶液变红.
(2)电解饱和食盐水总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
方案二:利用甲装置电解后的溶液,通过中和滴定来测定饱和食盐水的电解率.
(3)部分实验过程如下:
①用碱式滴定管(填“酸式滴定管”或“碱式滴定管”)量取10.00mL电解后的溶液,加入锥形瓶中;
②向锥形瓶中加入几滴酚酞试液,用0.2000mol•L-1标准盐酸滴定待测液,边滴边摇动锥形瓶,直到滴入最后一滴时,锥形瓶中溶液颜色由红色变无色,并保持半分钟不褪色时停止滴定;
③该小组所测实验数据如表:
未电解前饱和食盐水的物质的量浓度为5.4mol•L-1,经计算,求出该食盐水的电解率为7.4%.
④下列操作,会导致实验结果偏低的是AB(填序号).
A.滴定时锥形瓶中液滴飞溅出来
B.滴定前读数时平视,终点读数时俯视
C.锥形瓶用蒸馏水洗净后没用待测液润洗
D.酸式滴定管尖端气泡没有排除,滴定后消失.
[提示:饱和食盐水的电解率=(电解的氯化钠质量/总的氯化钠质量)×100%]
方案一:连接图甲、乙装置,在洗气瓶a中盛放足量的氢氧化钠溶液,通过测定洗气瓶a在电解前后的质量变化来计算饱和食盐水的电解率.

(1)正确的连接顺序为导管口B(填“A”或“B”)连导管口C,若事先往甲装置的饱和食盐水中滴入酚酞,则电解过程甲装置中铁棒(填“铁棒”或“碳棒”)附近的溶液变红.
(2)电解饱和食盐水总反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
方案二:利用甲装置电解后的溶液,通过中和滴定来测定饱和食盐水的电解率.
(3)部分实验过程如下:
①用碱式滴定管(填“酸式滴定管”或“碱式滴定管”)量取10.00mL电解后的溶液,加入锥形瓶中;
②向锥形瓶中加入几滴酚酞试液,用0.2000mol•L-1标准盐酸滴定待测液,边滴边摇动锥形瓶,直到滴入最后一滴时,锥形瓶中溶液颜色由红色变无色,并保持半分钟不褪色时停止滴定;
③该小组所测实验数据如表:
| 实验序号 | 盐酸体积(mL) |
| 第一组 | 19.90 |
| 第二组 | 24.70 |
| 第三组 | 20.10 |
| 第四组 | 20.00 |
④下列操作,会导致实验结果偏低的是AB(填序号).
A.滴定时锥形瓶中液滴飞溅出来
B.滴定前读数时平视,终点读数时俯视
C.锥形瓶用蒸馏水洗净后没用待测液润洗
D.酸式滴定管尖端气泡没有排除,滴定后消失.
4. CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义.
CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义.
(1)下列有关CO2说法不正确额是b(填字母)
a.CO2属于酸性氧化物
b.CO2是导致酸雨发生的主要原因
c.可用Na2CO3溶液捕捉(吸收)CO2
d.使用氢能源替代化石燃料可减少CO2排放
(2)金刚石和石墨燃烧反应中的能量变化如图所示.
①在通常情况下,金刚石和石墨中,石墨(填“金刚石”或“石墨”)更稳定.
②CO的燃烧热为283.0kJ•mol-1.
③石墨不完全燃烧生成CO的热化学方程式为C(s,石墨)+$\frac{1}{2}$O2(g)=CO(g)△H1=-110.5kJ•mol-1.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
计算298K时由C(s,石墨)和H2(g)生成1molC2H2(g)反应的焓变△H=+226.7kJ•mol-1.
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体.
已知某些化学键能数据如下表:
已知CO中的键为C≡O,则工业制备甲醇的热化学方程式为CO(g)+2H2 (g)?CH3OH(g)△H=-116kJ/mol.
 CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义.
CO2是一种主要的温室气体,研究CO2的利用对促进低碳社会的构建具有重要的意义.(1)下列有关CO2说法不正确额是b(填字母)
a.CO2属于酸性氧化物
b.CO2是导致酸雨发生的主要原因
c.可用Na2CO3溶液捕捉(吸收)CO2
d.使用氢能源替代化石燃料可减少CO2排放
(2)金刚石和石墨燃烧反应中的能量变化如图所示.
①在通常情况下,金刚石和石墨中,石墨(填“金刚石”或“石墨”)更稳定.
②CO的燃烧热为283.0kJ•mol-1.
③石墨不完全燃烧生成CO的热化学方程式为C(s,石墨)+$\frac{1}{2}$O2(g)=CO(g)△H1=-110.5kJ•mol-1.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的焓变进行推算.
已知:C(s,石墨)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
2H2(g)+O2(g)=2H2O(l)△H2=-571.6kJ•mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H3=-2599kJ•mol-1
计算298K时由C(s,石墨)和H2(g)生成1molC2H2(g)反应的焓变△H=+226.7kJ•mol-1.
(4)甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇气体.
已知某些化学键能数据如下表:
| 化学键 | C-C | C-H | H-H | C-O | C≡O | H-O |
| 键能/kJ•mol-1 | 348 | 413 | 436 | 358 | 1072 | 463 |