题目内容
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA | ||||
| B、室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | ||||
| C、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | ||||
D、5NH4NO3
|
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.铁与水蒸气反应生成的是四氧化三铁,根据电子守恒计算出生成氢气的物质的量及分子数;
B.氢氧化钠溶液的氢离子是水电离的,水电离的氢离子浓度为1×10-13mol/L;
C.氢氧燃料电池中,正极氧气得到电子,1mol氧气得到4mol电子;
D.该反应中,铵根离子中的氮原子被氧化成氮气,硝酸根离子中部分氮原子被氧化成氮气,生成4mol氮气转移了15mol电子.
B.氢氧化钠溶液的氢离子是水电离的,水电离的氢离子浓度为1×10-13mol/L;
C.氢氧燃料电池中,正极氧气得到电子,1mol氧气得到4mol电子;
D.该反应中,铵根离子中的氮原子被氧化成氮气,硝酸根离子中部分氮原子被氧化成氮气,生成4mol氮气转移了15mol电子.
解答:
解:A.0.2mol铁与水蒸气完全反应生成四氧化三铁,失去电子的物质的量为:(
-0)×0.2mol=
mol,根据电子守恒,生成氢气的物质的量为:
=
mol,生成的H2分子数目为
NA,故A错误;
B.室温下,1L pH=13的NaOH溶液中氢离子浓度为1×10-13mol/L,溶液中氢离子是水电离的,所以由水电离的OH-离子数目为10-13NA,故B错误;
C.氢氧燃料电池中,正极氧气得到电子,标况下22.4L氧气的物质的量为1mol,1mol氧气完全反应得到4mol电子,电路中通过的电子数目为4NA,故C错误;
D.该氧化还原反应中,生成4mol氮气转移了15mol电子,28g氮气的物质的量为1mol,生成1mol氮气转移的电子的物质的量为:
=3.75mol,转移的电子数目为3.75NA,故D正确;
故选D.
| 8 |
| 3 |
| 1.6 |
| 3 |
| ||
| 2 |
| 4 |
| 15 |
| 4 |
| 15 |
B.室温下,1L pH=13的NaOH溶液中氢离子浓度为1×10-13mol/L,溶液中氢离子是水电离的,所以由水电离的OH-离子数目为10-13NA,故B错误;
C.氢氧燃料电池中,正极氧气得到电子,标况下22.4L氧气的物质的量为1mol,1mol氧气完全反应得到4mol电子,电路中通过的电子数目为4NA,故C错误;
D.该氧化还原反应中,生成4mol氮气转移了15mol电子,28g氮气的物质的量为1mol,生成1mol氮气转移的电子的物质的量为:
| 15mol |
| 4 |
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系;选项D为难点和易错点,注意正确分析该反应中化合价变化情况.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
下表是某加碘盐包装袋上的部分文字说明:
根据这一说明某学生作出如下判断,其中正确的是( )
| 配料 | 氯化钠(NaCl)、碘酸钾(KIO3) |
| 含碘量 | (35±15)mg?kg-1(以I计) |
| 食用方法 | 菜未烧熟不宜加入加碘盐,菜烧熟后加入加碘盐最佳. |
| A、此食盐是纯净物 |
| B、“菜未烧熟不宜加入加碘盐”的原因可能是碘酸钾受热不稳定 |
| C、“加碘食盐”中的“碘”是指碘单质 |
| D、1kg此食盐中含碘酸钾(35±15)mg |
某溶液仅含K+、NH4+、Al3+、Fe2+、Mg2+、Ba2+、Cl-、NO3-、CO32-、SO42-中的4种离子,且所含离子的物质的量均为1mol.化学兴趣小组把溶液均匀分成四份,分别取样品进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).
③第三份加足量NaOH溶液加热后,没有气体生成,有沉淀生成
下列说法不正确的是( )
①第一份加入AgNO3溶液有沉淀产生
②第二份溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).
③第三份加足量NaOH溶液加热后,没有气体生成,有沉淀生成
下列说法不正确的是( )
| A、该溶液中所含的离子是:Fe2+、K+、SO42-、NO3- |
| B、实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为18g |
| C、若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| D、若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液会显血红色 |
某芳香族有机物的分子式为C8H6O2,它的分子结构(除苯环外不含其他环)中不可能是( )
| A、两个羟基 | B、一个醛基 |
| C、两个醛基 | D、一个羧基 |
化学与生产、生活息息相关,下列叙述错误的是( )
| A、铁表面镀锌可增强其抗腐蚀性 |
| B、用聚乙烯塑料代替聚乳酸塑料可减少白色污染 |
| C、大量燃烧化石燃料是造成雾霾天气的一种重要因素 |
| D、含重金属离子的电镀废液不能随意排放 |
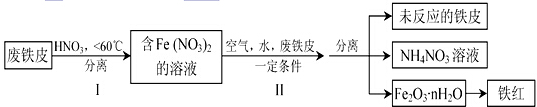
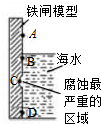 铁及其化合物与生产、生活关系密切.
铁及其化合物与生产、生活关系密切.