题目内容
某溶液仅含K+、NH4+、Al3+、Fe2+、Mg2+、Ba2+、Cl-、NO3-、CO32-、SO42-中的4种离子,且所含离子的物质的量均为1mol.化学兴趣小组把溶液均匀分成四份,分别取样品进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).
③第三份加足量NaOH溶液加热后,没有气体生成,有沉淀生成
下列说法不正确的是( )
①第一份加入AgNO3溶液有沉淀产生
②第二份溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).
③第三份加足量NaOH溶液加热后,没有气体生成,有沉淀生成
下列说法不正确的是( )
| A、该溶液中所含的离子是:Fe2+、K+、SO42-、NO3- |
| B、实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为18g |
| C、若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色 |
| D、若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液会显血红色 |
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:①第一份加入AgNO3溶液有沉淀产生,溶液中可能含有Cl-、CO32-、SO42-;
②第二份溶液中加入过量的稀硫酸,有气泡产生,该气体若为二氧化碳,说明溶液中含有CO32-,但是加入稀硫酸后碳酸根离子消失,所以产生的气体不是二氧化碳,应该为NO,原溶液中一定含有Fe2+、NO3-;由于加入了硫酸根离子,而溶液中阴离子种类不变,说明原溶液中一定含有SO42-,则一定不存在Ba2+;
③第三份加足量NaOH溶液加热后,没有气体生成,说明溶液中不存在NH4+,有沉淀生成,说明溶液中可能存在Mg2+;
由于所含离子的物质的量均为1mol,即含有1molFe2+、1molNO3-、1molSO42-,根据溶液电中性可知,溶液中还应该含有1mol带一个单位正电荷的阳离子,由于没有铵根离子存在,则溶液中一定含有K+,根据以上分析进行解答.
②第二份溶液中加入过量的稀硫酸,有气泡产生,该气体若为二氧化碳,说明溶液中含有CO32-,但是加入稀硫酸后碳酸根离子消失,所以产生的气体不是二氧化碳,应该为NO,原溶液中一定含有Fe2+、NO3-;由于加入了硫酸根离子,而溶液中阴离子种类不变,说明原溶液中一定含有SO42-,则一定不存在Ba2+;
③第三份加足量NaOH溶液加热后,没有气体生成,说明溶液中不存在NH4+,有沉淀生成,说明溶液中可能存在Mg2+;
由于所含离子的物质的量均为1mol,即含有1molFe2+、1molNO3-、1molSO42-,根据溶液电中性可知,溶液中还应该含有1mol带一个单位正电荷的阳离子,由于没有铵根离子存在,则溶液中一定含有K+,根据以上分析进行解答.
解答:
解:根据①可知,溶液中可能含有Cl-、CO32-、SO42-;
根据②加入过量的稀硫酸,有气泡产生,该气体如果为二氧化碳,说明溶液中含有CO32-,由于加入稀硫酸后碳酸根离子消失,改变了离子的种类,所以产生的气体一定不是二氧化碳,应该为NO,故原溶液中一定含有Fe2+、NO3-;由于加入了硫酸根离子,而溶液中阴离子种类不变,说明原溶液中一定含有SO42-,则一定不存在Ba2+;
根据③可知,溶液中不存在NH4+,由于存在亚铁离子,则加入氢氧化钠会有沉淀生成,溶液中也可能存在Mg2+;
由于所含4种离子的物质的量均为1mol,即:1molFe2+、1molNO3-、1molSO42-,根据溶液电中性可知,溶液中还应该含有1mol带一个单位正电荷的阳离子,③证明不存在铵根离子,则溶液中一定含有K+,
A.根据以上分析可知,该溶液中所含的离子是:Fe2+、K+、SO42-、NO3-,故A正确;
B.实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体为0.5mol氧化铁,其质量为160g/mol×0.5mol=80g,故B错误;
C.加入稀硫酸后,亚铁离子与稀硝酸反应生成一氧化氮气体,一氧化氮遇到空气变成红棕色气体,故C正确;
D.由于溶液中存在硝酸根离子和亚铁离子,若向溶液中加入稀硫酸和和KSCN溶液,硝酸根离子在酸性条件下能够将亚铁离子氧化成铁离子,铁离子与硫氰根离子反应生成血红色的硫氰化铁,故D正确;
故选B.
根据②加入过量的稀硫酸,有气泡产生,该气体如果为二氧化碳,说明溶液中含有CO32-,由于加入稀硫酸后碳酸根离子消失,改变了离子的种类,所以产生的气体一定不是二氧化碳,应该为NO,故原溶液中一定含有Fe2+、NO3-;由于加入了硫酸根离子,而溶液中阴离子种类不变,说明原溶液中一定含有SO42-,则一定不存在Ba2+;
根据③可知,溶液中不存在NH4+,由于存在亚铁离子,则加入氢氧化钠会有沉淀生成,溶液中也可能存在Mg2+;
由于所含4种离子的物质的量均为1mol,即:1molFe2+、1molNO3-、1molSO42-,根据溶液电中性可知,溶液中还应该含有1mol带一个单位正电荷的阳离子,③证明不存在铵根离子,则溶液中一定含有K+,
A.根据以上分析可知,该溶液中所含的离子是:Fe2+、K+、SO42-、NO3-,故A正确;
B.实验③,充分反应后,过滤、洗涤、灼烧,最终所得固体为0.5mol氧化铁,其质量为160g/mol×0.5mol=80g,故B错误;
C.加入稀硫酸后,亚铁离子与稀硝酸反应生成一氧化氮气体,一氧化氮遇到空气变成红棕色气体,故C正确;
D.由于溶液中存在硝酸根离子和亚铁离子,若向溶液中加入稀硫酸和和KSCN溶液,硝酸根离子在酸性条件下能够将亚铁离子氧化成铁离子,铁离子与硫氰根离子反应生成血红色的硫氰化铁,故D正确;
故选B.
点评:本题考查了常见离子的检验、离子共存的判断,题目难度中等,注意掌握常见离子的化学性质及检验方法,能够根据电荷守恒平衡溶液中未知离子的存在情况,正确理解题干信息是解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
化学与以节能减排为基础的低碳经济密切相关.下列做法违背发展低碳经济的是( )
| A、城市采用分质供水,收集雨水进行综合利用 |
| B、推广煤的气化、液化技术,提供清洁高效燃料 |
| C、大力发展汽车产业,鼓励市民购买家用汽车 |
| D、开发利用太阳能、风能、氢能、核能等能源 |
下列说法不正确的是( )
| A、能用酒精、汽油将洒在衣服上的油汤除去,实际上是用萃取的原理 |
| B、从热饱和FeSO4溶液中得到FeSO4?7H2O晶体的操作是冷却结晶 |
| C、实验测得1mol某气体体积为22.4L,测定条件一定是标准状况 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
苹果酸的结构简式为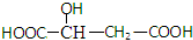 ,下列说法正确的是( )
,下列说法正确的是( )
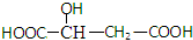 ,下列说法正确的是( )
,下列说法正确的是( )| A、苹果酸中能发生酯化反应的官能团有2种 |
| B、1mol苹果酸可与3mol NaOH发生中和反应 |
| C、1mol苹果酸与足量金属Na反应生成1mol H2 |
D、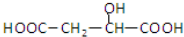 与苹果酸互为同分异构体 与苹果酸互为同分异构体 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA | ||||
| B、室温下,1L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | ||||
| C、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | ||||
D、5NH4NO3
|
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A、1mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、2L 0.5mol?L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C、1mol Na2O2固体中含离子总数为4NA |
| D、丙烯和环丙烷组成的42g混合气体中氢原子的个数为6NA |
下列操作中不正确的是( )
| A、过滤时,玻璃棒与三层滤纸的一边接触 |
| B、过滤时,漏斗下方紧贴烧杯内壁 |
| C、加热试管内固体物质时,试管口要略微向下倾斜 |
| D、向试管中滴加液体时,胶头滴管紧贴试管内壁 |
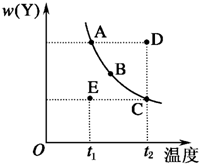 对于2X(g)?Y(g)的反应体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态).
对于2X(g)?Y(g)的反应体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态).