题目内容
为测定某工厂制得的漂白粉中有效成分的含量,某小组进行了如下实验:称取漂白粉2.0g,研磨后溶解,配置成250mL溶液,取出25.00mL加入到锥形瓶中,再加入过量的KI溶液和过量的硫酸,此时发生的离子方程式为: ,静置.待完全反应后,用0.1mol?L-1的Na2S2O3溶液做标准溶液滴定反应生成的碘,已知反应式为:2Na2S2O3+I2=Na2S4O6+2NaI,共用去 Na2S2O3溶液20.00mL.则该漂白粉中有效成分的质量分数为 (保留到小数点后两位).
考点:化学方程式的有关计算
专题:计算题
分析:ClO-具有强氧化性,酸性条件下,将I-氧化为I2,自身被还有为Cl-,同时生成H2O,发生离子反应为:2I-+ClO-+2H+=I2+Cl-+H2O,结合2Na2S2O3+I2=Na2S4O6+2NaI,可得关系式Ca(ClO)2~2I2~4Na2S2O3,据此计算n[Ca(ClO)2],根据m=nM计算次氯酸钙的质量,进而计算次氯酸钙的质量分数.
解答:
解:加入过量的KI溶液和过量的硫酸与漂白粉溶液,发生离子反应为:2I-+ClO-+2H+=I2+Cl-+H2O,由2Na2S2O3+I2=Na2S4O6+2NaI,可得关系式Ca(ClO)2~2I2~4Na2S2O3,n[Ca(ClO)2]=
n(Na2S2O3)=20.0 mL×10-3 L?mL-1×0.1 mol?L-1×
=0.005 mol,
Ca(ClO)2%=
×100%=35.75%,
故答案为:2I-+ClO-+2H+=I2+Cl-+H2O;35.75%.
| 1 |
| 4 |
| 250mL |
| 25mL |
Ca(ClO)2%=
| 0.005mol×143g/mol |
| 2.0g |
故答案为:2I-+ClO-+2H+=I2+Cl-+H2O;35.75%.
点评:本题考查氧化还原反应滴定计算,注意利用关系式进行计算,难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
①正常雨水的pH为7.0,酸雨的pH小于7.0;
②严格执行机动车尾气排放标准有利于防止大气污染;
③使用二氧化硫和某些含硫化合物进行增白的食品会损害人体健康;
④食品厂产生的含丰富氮、磷营养素的废水可长期排向养鱼水库.
①正常雨水的pH为7.0,酸雨的pH小于7.0;
②严格执行机动车尾气排放标准有利于防止大气污染;
③使用二氧化硫和某些含硫化合物进行增白的食品会损害人体健康;
④食品厂产生的含丰富氮、磷营养素的废水可长期排向养鱼水库.
| A、①③ | B、①④ | C、②③④ | D、②③ |
下列化学用语使用正确的是( )
| A、石英的化学式:CaCO3 |
B、CO2的电子式: |
| C、HClO的结构式:H-O-Cl |
D、Mg2+的结构示意图: |
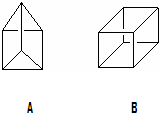 有机物A和B都是重要的化工原料,认真观察A和B的结构回答下列问题:
有机物A和B都是重要的化工原料,认真观察A和B的结构回答下列问题: 仔细观察图A、B两个装置,两个烧杯分别盛有足量的CuSO4溶液,回答问题:
仔细观察图A、B两个装置,两个烧杯分别盛有足量的CuSO4溶液,回答问题: