题目内容
分别完全燃烧①1molCH4、②1molC2H4、③1molC6H6,生成的水相等的是 ; 需要的氧气最多的是 .(填序号)
考点:化学方程式的有关计算
专题:烃及其衍生物的燃烧规律
分析:各烃的物质的量相等,生成的水相等,则烃分子中H原子数目相等,需要的氧气最多,根据1molCxHy的耗氧量(x+
)mol计算判断.
| y |
| 4 |
解答:
解:各烃的物质的量相等,完全燃烧生成的水相等,则烃分子中H原子数目相等,故CH4、2H4符合;
①1molCH4耗氧量为(1+
)mol=2mol,②1molC2H4耗氧量为(2+
)mol=3mol,③1molC6H6耗氧量为(6+
)mol=7.5mol,故需要的氧气最多的是C6H6,
故答案为:①②;③.
①1molCH4耗氧量为(1+
| 4 |
| 4 |
| 4 |
| 4 |
| 6 |
| 4 |
故答案为:①②;③.
点评:本题考查烃燃烧有关计算,难度不大,注意根据烃燃烧通式理解耗氧量问题.

练习册系列答案
相关题目
下列家庭化学小实验不能达到预期目的是( )
| A、用热的纯碱溶液洗涤粘有油脂的餐具 |
| B、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
| C、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| D、用灼烧方法鉴别羊毛布料和纯棉布料 |
下列实验能够达到实验目的是( )
A、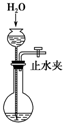 检查装置的气密性 |
B、 制备并观察氢氧化亚铁 |
C、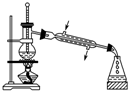 除去溴苯中的苯 |
D、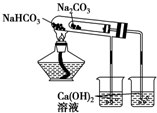 比较NaHCO3和NaCO3热稳定性 |
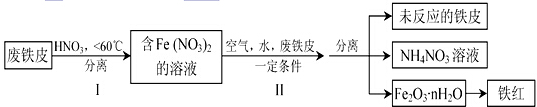
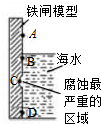 铁及其化合物与生产、生活关系密切.
铁及其化合物与生产、生活关系密切.