题目内容
1.下列物质中属于电解质,且能导电的是( )| A. | 熔融的氢氧化钾 | B. | 液态铜 | C. | 液态氯化氢 | D. | 固态氯化钾 |
分析 在水溶液或熔化状态下能导电的化合物为电解质,有自由移动电子或离子的物质能导电,以此来解答,注意电解质和非电解质都是化合物,既要排除单质又要排除混合物.
解答 解:A.熔融的氢氧化钾中有自由移动的离子,能导电,是化合物,则属于电解质,故A正确;
B.液态铜是单质,故不属于电解质,故B错误;
C.液态HCl中没有自由移动的离子,不导电;但HCl溶于水在水分子的作用下能电离出氯离子和氢离子,属于电解质,故C错误;
D.固态氯化钾中没有自由移动的离子,不导电;但氯化钾晶体为离子化合物,在水溶液中或熔融状态下能导电,属于电解质,故D错误;
故选A.
点评 本题考查了电解质的判断,难度不大,注意电解质和非电解质都必须是化合物,单质和混合物既不是电解质也不是非电解质,离子晶体在固体时不导电.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.在t℃时,将0.2mol X和0.8mol Y充入密闭容器中,当反应X(g)+Y(g)?nZ(g)+R(g)达到平衡时,若将反应混合气体中各物质浓度均增大一倍,X的转化率不变,并知c(X)c(Y)=c(Z)nc(R),则X的转化率为( )
| A. | 80% | B. | 65% | C. | 45% | D. | 37% |
12.已知298K下反应2Al2O3(s)+3C(s)═4Al(s)+3CO2(g)△H=+2 171kJ/mol,△S=+635.5J/(mol•K),则下列说法正确的是( )
| A. | 由题给△H值可知,该反应是一个放热反应 | |
| B. | △S>0表明该反应是一个熵增加的反应 | |
| C. | 该反应在室温下可能自发 | |
| D. | 不能确定该反应能否自发进行 |
6.下列实验现象,与新制氯水中的某些成分(括号内物质)没有关系的是( )
| A. | 将石灰石加入新制氯水中,固体逐渐溶解(H+) | |
| B. | 向FeCl2溶液中滴加氯水,再滴加KSCN溶液,发现呈红色(Cl2) | |
| C. | 使红色布条褪色(HCl) | |
| D. | 滴加AgNO3溶液生成白色沉淀(Cl-) |
13.在1L 0.5mol/L NaCl中,含有的Na+数约是( )
| A. | 3.01×1023 | B. | 6.02×1023 | C. | 0.5 | D. | 1 |
10.若20g密度为ρ g•cm-3的Ca(NO3)2溶液里含1g Ca2+,则NO${\;}_{3}^{-}$的物质的量浓度是(mol/L)( )
| A. | $\frac{ρ}{400}$ | B. | $\frac{20}{ρ}$ | C. | 2.5 ρ | D. | 1.25 ρ |
11.不能用H++OH-=H2O来表示的化学反应是( )
| A. | NaOH溶液与盐酸反应 | B. | KOH溶液与稀硫酸反应 | ||
| C. | Ba(OH)2溶液与稀硫酸反应 | D. | 澄清石灰水与稀硝酸反应 |
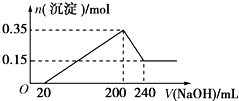 将一定质量的镁铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.
将一定质量的镁铝混合物投入200mL硫酸中,固体全部溶解后,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.