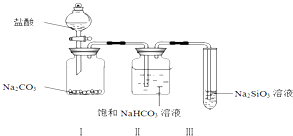
题目内容
3.下列气体不能用排空气法收集的是( )| A. | O2 | B. | NH3 | C. | NO | D. | CO |
分析 排空气法适合收集密度与空气密度相差较大的气体,若密度比空气的大,采用向上排空气法,若密度比空气的小,采用向下排空气法,密度与空气密度接近的不能用排气法收集.
解答 解:A.氧气密度大于空气密度,可以用向上排空气法收集,故A不选;
B.氨气密度小于空气密度,可以用向下排空气法收集,故A不选;
C.一氧化氮不稳定,能与空气中的氧气反应生成二氧化氮,且密度与空气密度接近,不能用排气法收集,故C选;
D.CO的密度和空气密度相差不大,不能用排空气法收集,故D选;
故选:CD.
点评 本题考查气体的收集方法,明确气体的性质是解题关键,注意排气法适合收集密度与空气密度相差较大的气体,注意NO、CO密度与空气密度相近,所以不能用排空气法收集.

练习册系列答案
相关题目
13.短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
| A. | 元素X 的简单气态氢化物的热稳定性比W 的弱 | |
| B. | 原子半径的大小顺序:rY>rZ>rW>rX | |
| C. | 化合物YX、ZX2、WX3 中化学键的类型相同 | |
| D. | 最高价氧化物对应水化物的酸性:W比Z 的弱 |
14.下列说法正确的是( )
| A. | 分子内共价键越强,分子越稳定,其熔沸点也越高 | |
| B. | 离子键的本质就是阴、阳离子之间的相互吸引 | |
| C. | 变化过程中化学键被破坏,则一定发生化学变化 | |
| D. | 由原子构成的晶体可能是原子晶体,也可能是分子晶体 |
11.下列各组物质的水溶液不用其它试剂无法鉴别出来的是( )
| A. | NaOH、AlCl3 | B. | CuSO4、BaCl2 | C. | NaAlO2、HCl | D. | MgCl2、NaOH |
18.将①中溶液逐滴滴入②中,预测的现象与实际相符的是( )
| 选项 | ①中物质 | ②中物质 | 预测②中的现象 |
| A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
| B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生大量红棕色气体 |
| C | 氯化铁溶液 | 苯酚水溶液 | 溶液变成紫色 |
| D | 氨水 | 氯化铝溶液 | 立即生成白色沉淀,最终沉淀逐渐溶解 |
| A. | A | B. | B | C. | C | D. | D |
8.常用一些图案标示危险化学品,化学物质与其图案标识相符的是( )
| A. |  氮气 | B. |  铜片 | C. |  浓盐酸 | D. |  浓硝酸 |
13.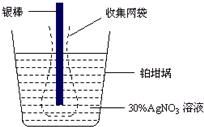 精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )
精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )
 精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )
精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量.实际测量中常用的银电量计结构如图所示,则下列说法正确的是( )| A. | 电量计中的银棒应与电源的正极相连,铂棒上发生的电极反应式为:2H++NO3-+e-=NO2↑+H2O | |
| B. | 已知每摩尔电子的电量为96 500 C,若反应进行10分钟,称量电解前后铂坩埚的质量变化值为108.0 mg,则电解过程中的平均电流约为9.65A | |
| C. | 若要测定电解精炼铜时通过的电量,可将银电量计中的银棒与待测电解池的精铜电极相连 | |
| D. | 实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂坩埚而导致测量误差,常在银电极附近增加一个收集网袋.若没有收集网袋,测量结果会偏低 |