题目内容
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳。其中一种镁电池的反应为:x Mg+Mo3S4 MgxMo3S4
MgxMo3S4
下列说法错误的是
| A.放电时Mg2+向正极迁移 |
| B.放电时正极反应为:Mo3S4+2xe-=Mo3S42x- |
| C.充电时Mo3S4发生氧化反应 |
| D.充电时阴极反应为:Mg2++2e-=Mg |
C
解析试题分析:该反应为可充电电池,先分清充电(原电池)和放电(电解池)两个过程,然后用双线桥法标出,分别写出正负极反应,然后判断产物,电子、离子流向等相关知识。C、充电时,Mo3S4,为生成物,故错误。
考点:考查电化学基础知识,涉及原电池和电解池的电极判断,电极反应书写,离子流向等相关知识。

练习册系列答案
相关题目
下列有关金属的说法正确的是
| A.银器在空气中变暗后一定条件下被还原又会变光亮 |
| B.当镀锌铁制品的镀层破损后,镀层不能对铁制品起保护作用 |
| C.不锈钢不生锈是因为表面有保护膜 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
用石墨电极电解下列溶液,电解后要恢复原溶液加入物质是原溶质的是( )
| A.Na2SO4溶液 | B.NaOH溶液 | C.CuCl2溶液 | D.H2SO4溶液 |
在下图装置中,若通电一段时间后乙装置左侧电极质量增加,则下列说法错误的是( )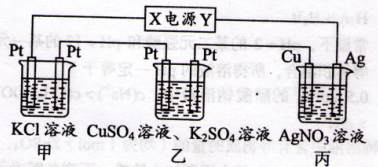
| A.乙中左侧电极反应式:Cu2++2e-=Cu |
| B.电解过程中装置丙的pH无变化 |
| C.向甲中通人适量的HCl气体,可使溶液恢复到电解前的状态 |
| D.当甲装置中产生标准状况下4.48 L气体时,Cu电极上质量增加43.2 g |
镁—次氯酸盐燃料电池具有比能量高、安全方便等优点,该电池主要工作原理如图所示,其正极反应为:ClO-+H2O+2e-=Cl-+2OH-,关于该电池的叙述正确的是
| A.该电池中镁为负极,发生还原反应 |
| B.电池工作时,OH-向正极移动 |
| C.电池工作时,正极周围溶液的pH将不断变小 |
| D.该电池的总反应式为:Mg+ClO-+H2O=Mg(OH)2↓+Cl- |
一定条件下,碳钢腐蚀与溶液pH的关系如下:
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | |||
下列说法不正确的是( )
A.在pH<4溶液中,碳钢主要发生析氢腐蚀
B.在pH>6溶液中,碳钢主要发生吸氧腐蚀
C.在pH>14溶液中,碳钢腐蚀的正极反应为O2+4H++4e—=2H2O
D.在煮沸除氧气后的碱性溶液中,碳钢腐蚀速率会减缓
有关下列四个常用电化学装置的叙述中,正确的是
 |  |  |  |
| 图Ⅰ 碱性锌锰电池 | 图Ⅱ 铅-硫酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
A.图Ⅰ所示电池中,MnO2的作用是催化剂
B.图II所示电池放电过程中,硫酸浓度不断增大
C.图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图IV所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
关于下列装置说法正确的是 
| A.装置①中,盐桥中的K+移向ZnSO4溶液 |
| B.装置②工作一段时间后,a极附近溶液的pH增大 |
| C.用装置③精炼铜时,c极为粗铜 |
| D.装置④中电子由Zn流向Sn,Sn为正极有气泡生成 |
