题目内容
有关下列四个常用电化学装置的叙述中,正确的是
 | 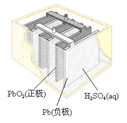 |  |  |
| 图Ⅰ 碱性锌锰电池 | 图Ⅱ 铅-硫酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
A.图Ⅰ所示电池中,MnO2的作用是催化剂
B.图II所示电池放电过程中,硫酸浓度不断增大
C.图III所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D.图IV所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
D
解析试题分析:A、MnO2的作用是氧化剂,错误;B、Pb+PbO2+2H2SO4=2PbSO4+2 H2O,H2SO4被消耗,浓度减小,错误;C、粗铜含杂质,溶解的铜小于镀上的铜,Cu2+浓度减小;D、负极Zn--Zn2+ 氧化反应,做还原剂;正极Ag2O- Ag 还原反应,Ag2O是氧化剂,正确。
考点:考查原电池和电解池等相关知识。

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
利用下图密封装置进行实验,起初a、b两处液面相平,放置一段时间。下列说法正确的是
| A.a中发生析氢腐蚀,b中发生吸氧腐蚀 |
| B.一段时间后,a中液面低于b中液面 |
| C.a中溶液的pH增大,b中溶液的pH减小 |
| D.a、b中负极的电极反应式均为Fe-2e-=Fe2+ |
镁及其化合物一般无毒(或低毒)、无污染,且镁原电池放电时电压高而平稳。其中一种镁电池的反应为:x Mg+Mo3S4 MgxMo3S4
MgxMo3S4
下列说法错误的是
| A.放电时Mg2+向正极迁移 |
| B.放电时正极反应为:Mo3S4+2xe-=Mo3S42x- |
| C.充电时Mo3S4发生氧化反应 |
| D.充电时阴极反应为:Mg2++2e-=Mg |
关于下图装置的叙述中正确的是( )
| A.电流由铁钉经过导线流向石墨棒 |
| B.该装置是一个简易的电解饱和食盐水的装置 |
C.石墨棒上发生的电极反应式: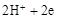 → →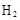 ↑ ↑ |
D.石墨棒上发生的电极反应式: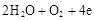 → →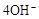 |
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,电解总反应:2Cu+H2O=Cu2O+H2下列说法正确的是
| A.石墨电极上产生氢气 |
| B.铜电极发生还原反应 |
| C.铜电极接直流电源的负极 |
| D.当有0.1mol电子转移时,有0.1molCu2O生成。 |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水” 电池在海水中放电时的有关说法正确的是( )。
| A.正极反应式:Ag+Cl--e-=AgCl |
| B.每生成1 mol Na2Mn5O10转移2 mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |
下图为某太空站的能量转化示意图,其中燃料电池用KOH溶液为电解液。下列说法不正确的是。 
| A.水电解系统中,加入Na2 SO4可增加溶液导电性 |
| B.燃料电池的负极反应:H2+2OH一一2 e一="2" H2O |
| C.整个系统实现了物质零排放及能量间完全转化 |
D.该系统发生总反应:2H2+O2  2 H2O 2 H2O |
用Pt做电极,电解含C(Cu2+): C(Na+): C(Cl-)=1:2:4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是
| A.阴极:2H++2e-=H2↑阳极:4OH-- 4e-=2H2O+O2↑ |
| B.阴极:2H++2e-=H2↑阳极:2Cl--2e-=Cl2↑ |
| C.阴极:Cu2++2e-=Cu阳极:4OH-- 4e-=2H2O+O2↑ |
| D.阴极:Cu2++2e-="Cu" 阳极:2Cl--2e-=Cl2↑ |
某实验兴趣小组用如图所示装置实验,其中描述不合理的是
| A.Zn为负极 |
| B.H+向负极定向移动 |
| C.化学能转化为电能 |
| D.Cu电极反应:2H++2e-=H2↑ |