题目内容
13.短周期主族元素X、Y、Z在周期表中的位置如图所示.下列说法正确的是( )| Z | |
| X | Y |
| A. | Z元素的最高正化合价,一定等于其主族序数 | |
| B. | 它们的原子半径由大到小的顺序一定是Y>X>Z | |
| C. | 若它们的原子最外层电子数之和为11,则它们均为非金属元素 | |
| D. | 若它们均为非金属元素,则X与氧元素组成的物质一定是酸性氧化物 |
分析 由短周期主族元素X、Y、Z在周期表中的位置,可知Z为第二周期元素,X、Y为第三周期元素,
A.Z为O或F时,无正价;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小;
C.它们的原子最外层电子数之和为11,设X的最外层电子数为x,则x+(x+1)×2=11,解得x=3;
D.若它们均为非金属元素,X为Si或P或S.
解答 解:A.Z为O或F时,无正价,若为N时最高正化合价一定等于其主族序数,故A错误;
B.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径由大到小的顺序一定是X>Y>Z,故B错误;
C.它们的原子最外层电子数之和为11,设X的最外层电子数为x,则x+(x+1)×2=11,解得x=3,则X为Al,Al为金属元素,故C错误;
D.若它们均为非金属元素,X为Si或P或S,二氧化硅、五氧化二磷、二氧化硫或三氧化硫均为酸性氧化物,故D正确;
故选D.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意选项D中酸性氧化物的判断,题目难度不大.

练习册系列答案
相关题目
14.下列关于多电子原子的核外电子的运动规律的叙述正确的是( )
| A. | 核外电子是分层运动的 | |
| B. | 所有电子在同一区域里运动 | |
| C. | 能量高的电子在离核近的区域里运动 | |
| D. | 能量低的电子在离核远的区域里运动 |
1.常温下将盛有10mL NO2和10mL NO的混合气体的试管倒立于水槽中并向其中通入O2,一段时间后,试管内还剩余2mL气体,则通入O2的体积可能为( )
| A. | 8mL | B. | 8.5mL | C. | l0mL | D. | 10.5mL |
8.下列叙述正确的是( )
| A. | HBr、HI、HCl的稳定性依次减弱 | B. | RbOH、KOH、NaOH的碱性依次增强 | ||
| C. | K+、Na+、Li+的氧化性依次减弱 | D. | HIO4、HBrO4、HClO4的酸性依次增强 |
18.下列说法正确的是( )
| A. | 乙烯和聚乙烯均能使溴水褪色 | |
| B. | 乙酸和乙酸乙酯均能发生取代反应 | |
| C. | 甲烷、苯和油脂均不能使酸性KMnO4溶液褪色 | |
| D. | 葡萄糖与果糖、淀粉与纤维素分子式相同,均互为同分异构体 |
5.下列关于有机化合物的说法正确的是( )
| A. | 乙酸和乙酸乙酯可用Na2CO3溶液加以区别 | |
| B. | 戊烷有两种同分异构体 | |
| C. | 乙烯、聚乙烯和苯分子均含有碳碳双键 | |
| D. | 糖类、油脂和蛋白质均可发生水解反应 |
2.常温下,下列溶液可用铁制或铝制容器盛装的是( )
| A. | 浓盐酸 | B. | 浓硝酸 | C. | 稀硫酸 | D. | 稀盐酸 |
3.下列说法正确的是( )
| A. | 活化分子间的碰撞一定发生化学反应 | |
| B. | 吸热反应只有加热才能发生 | |
| C. | 有能量变化的一定是化学反应 | |
| D. | 有化学键断裂不一定发生化学反应 |

 .
.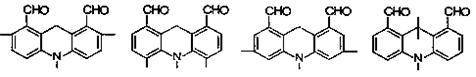 .
. 结构;
结构;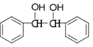 写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)
写出制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)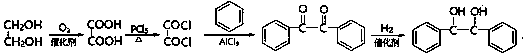 .
.