题目内容
20.昆石属于稀有的石种,其成分主要是二氧化硅以及铁、钠、钙元素的氧化物,根据图示流程回答有关问题.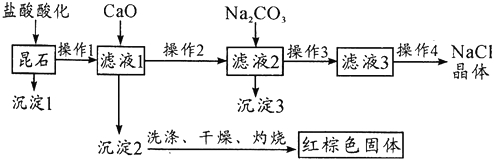
(1)操作1和操作4的名称分别是过滤 和蒸发结晶
(2)写出加CaO时发生反应的离子方程式:CaO+H2O=Ca2++2OH-、CaO+2H+=Ca2++H2O、Fe3++3OH-=Fe(OH )3↓
(3)在沉淀2后,依次进行了洗涤、干燥、灼烧操作,证明沉淀已经洗涤干净的操作是取洗涤液少许于试管中滴入硝酸酸化的硝酸银溶液,若无沉淀证明已经洗涤干净
(4)证明滤液3含有钠元素的方法是用铂丝蘸取滤液3,放在酒精灯的外焰灼烧,火焰呈黄色,证明含有钠元素
(5)写出能证明红棕色固体中含有金属元素的操作过程、现象、结论.取红棕色固体少许,用盐酸溶解,滴入2滴KSCN溶液,溶液变为红色,证明含有金属铁元素.
分析 昆石加入盐酸,生成钠盐、铁盐、钙盐,过滤除去二氧化硅,加入CaO调节pH,红棕色固体为Fe(OH)3,加入Na2CO3沉淀Ca2+,过滤得到NaCl溶液,蒸发结晶得到NaCl晶体;
(1)操作1之后出现沉淀和滤液,则操作1是过滤;操作4出现晶体,则操作4是蒸发结晶;
(2)加CaO时,CaO和H2O反应生成氢氧化钙,CaO调节pH生成Fe(OH)3沉淀,离子方程式为:CaO+H2O=Ca2++2OH-、CaO+2H+→Ca2++H2O、Fe3++3OH-→Fe(OH )3↓;
(3)FeCl3水解生成Fe(OH)3,沉淀中附着Cl-,可以检验Cl-来判断沉淀是否已经洗涤干净;
(4)钠元素不能生成沉淀,常用焰色反应检验钠元素;
(5)红棕色固体为Fe(OH)3,证明是否含有Fe3+,首先取红棕色固体少许,用盐酸溶解,滴入2滴KSCN溶液检验.
解答 解:(1)操作1之后出现沉淀和滤液,则操作1是过滤;操作4出现晶体,则操作4是蒸发结晶,故答案为:过滤;蒸发结晶;
(2)加CaO时,CaO和H2O反应生成氢氧化钙,CaO调节pH生成Fe(OH)3沉淀,离子方程式为CaO+H2O=Ca2++2OH-、CaO+2H+=Ca2++H2O、Fe3++3OH-=Fe(OH )3↓,
故答案为:CaO+H2O=Ca2++2OH-、CaO+2H+=Ca2++H2O、Fe3++3OH-=Fe(OH )3↓;
(3)FeCl3水解生成Fe(OH)3,沉淀中附着Cl-,可以检验Cl-来判断沉淀是否已经洗涤干净,其操作为取洗涤液少许于试管中滴入硝酸酸化的硝酸银溶液,若无沉淀证明已经洗涤干净;
故答案为:取洗涤液少许于试管中滴入硝酸酸化的硝酸银溶液,若无沉淀证明已经洗涤干净;
(4)钠元素不能生成沉淀,常用焰色反应检验钠元素,操作为用铂丝蘸取滤液3,放在酒精灯的外焰灼烧,火焰呈黄色,证明含有钠元素,
故答案为:用铂丝蘸取滤液3,放在酒精灯的外焰灼烧,火焰呈黄色,证明含有钠元素;
(5)红棕色固体为Fe(OH)3,证明是否含有Fe3+,首先取红棕色固体少许,用盐酸溶解,滴入2滴KSCN溶液,溶液变为红色,证明含有金属铁元素,
故答案为:取红棕色固体少许,用盐酸溶解,滴入2滴KSCN溶液,溶液变为红色,证明含有金属铁元素.
点评 本题考查二氧化硅以及铁、钠、钙元素的氧化物的性质,难度不大,涉及实验操作及元素的检验.

 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案PCl5(g)?PCl3(g)+Cl2(g)
| 编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
| PCl5(g) | PCl3(g) | Cl2(g) | |||
| Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
| Ⅱ | 320 | 0.80 | t2 | ||
| Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
| A. | 平衡常数K:容器Ⅱ>容器Ⅲ | |
| B. | 反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ | |
| C. | 反应到达平衡时,容器I中的平均速率为v(PCl5)=$\frac{0.10}{{t}_{1}}$mol/(L•s) | |
| D. | 起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行 |
| A. | 分子中三个碳原子可能处在同一直线上 | |
| B. | 它的五氯代物数目与三氯代物的数目相等 | |
| C. | 它属于烃类 | |
| D. | 该物质易溶于水,难溶于有机物 |
| A. | 温度、体积不变,充入氩气 | B. | 条件不变,对体系加热 | ||
| C. | 温度、体积不变,充入氯气 | D. | 温度不变,增大容器体积 |
| A. | H2 | B. | CO | C. | C12H22O11 | D. | C6H12O6 |
 ④
④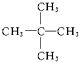 ⑤
⑤ ⑥CH3-CH═CH2 ⑦
⑥CH3-CH═CH2 ⑦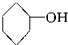 ⑧
⑧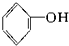 ⑨
⑨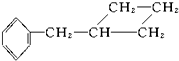 中,属于环状化合物的是③⑤⑦⑧⑨,属于脂环化合物的是⑤⑦,属于芳香化合物的是③⑧⑨,属于脂肪烃的是①②④⑥.
中,属于环状化合物的是③⑤⑦⑧⑨,属于脂环化合物的是⑤⑦,属于芳香化合物的是③⑧⑨,属于脂肪烃的是①②④⑥. 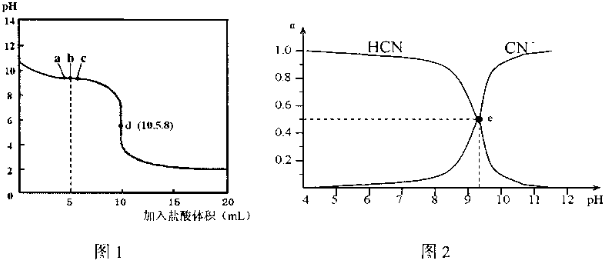
| A. | b点时,溶液中微粒浓度大小的关系:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+) | |
| B. | d点溶液存在的关系:c(Na+)+c(H+)=c(HCN)+c(OH-)+2c(CN-) | |
| C. | 图2中的e点对应图1中的c点 | |
| D. | 在滴定过程中选用酚酞试剂比选用甲基橙试剂作指示剂误差更小 |
 苯甲酸叶醇酯存在于麝香、百合和水仙花中,可用于高档香水的香精配方中,留香时间超过两周,其结构简式如图所示,下列关于苯甲酸叶醇酯的说法中错误的是( )
苯甲酸叶醇酯存在于麝香、百合和水仙花中,可用于高档香水的香精配方中,留香时间超过两周,其结构简式如图所示,下列关于苯甲酸叶醇酯的说法中错误的是( )| A. | 苯甲酸叶醇酯能发生氧化反应 | |
| B. | 苯甲本叶醇酯能使溴的四氯化碳溶液褪色 | |
| C. | 1mol苯甲酸叶醇酯最多能与4molH2发生加成反应 | |
| D. | 1mol苯甲酸叶醇酯与NaOH溶液反应时,能消耗2molNaOH |