题目内容
有A、B、C、D和E五瓶无色溶液,他们是中学化学中常用的无机试剂,他们的阴、阳离子均不同.现进行如下实验:
①A与E、B与D反应均能产生不溶于稀硝酸的白色沉淀;
②B与C、D、E反应时,均有沉淀生成,且B过量时,D中的沉淀部分溶解;
③B与C、C与D反应生成的沉淀均可溶于A;
④C的焰色反应呈黄色,往C中滴入少量A,有无色、无味的气体生成.
则:(写出溶质的化学式)
A. B. C. D. E. .
①A与E、B与D反应均能产生不溶于稀硝酸的白色沉淀;
②B与C、D、E反应时,均有沉淀生成,且B过量时,D中的沉淀部分溶解;
③B与C、C与D反应生成的沉淀均可溶于A;
④C的焰色反应呈黄色,往C中滴入少量A,有无色、无味的气体生成.
则:(写出溶质的化学式)
A.
考点:物质的检验和鉴别的实验方案设计,几组未知物的检验
专题:物质检验鉴别题
分析:①A与E、B与D反应均能产生不溶于稀硝酸的白色沉淀,白色沉淀分别为氯化银、硫酸钡;
②B与C、D、E反应时,均有沉淀生成,且B过量时,D中的沉淀部分溶解,则B为氢氧化钡,D为硫酸铝;
③B与C、C与D反应生成的沉淀均可溶于A,则A为HCl,沉淀分别为碳酸钡、氢氧化铝;
④C的焰色反应呈黄色,往C中滴入少量A,有无色、无味的气体生成,则气体为二氧化碳,C中含Na元素,C为NaHCO3,以此来解答.
②B与C、D、E反应时,均有沉淀生成,且B过量时,D中的沉淀部分溶解,则B为氢氧化钡,D为硫酸铝;
③B与C、C与D反应生成的沉淀均可溶于A,则A为HCl,沉淀分别为碳酸钡、氢氧化铝;
④C的焰色反应呈黄色,往C中滴入少量A,有无色、无味的气体生成,则气体为二氧化碳,C中含Na元素,C为NaHCO3,以此来解答.
解答:
解:①A与E、B与D反应均能产生不溶于稀硝酸的白色沉淀,白色沉淀分别为氯化银、硫酸钡;
②B与C、D、E反应时,均有沉淀生成,且B过量时,D中的沉淀部分溶解,则B为氢氧化钡,D为硫酸铝;
③B与C、C与D反应生成的沉淀均可溶于A,则A为HCl,沉淀分别为碳酸钡、氢氧化铝;
④C的焰色反应呈黄色,往C中滴入少量A,有无色、无味的气体生成,则气体为二氧化碳,C中含Na元素,C为NaHCO3,
由上述分析可知A为HCl,B为Ba(OH)2,C为NaHCO3,D为Al2(SO4)3,E为AgNO3,
故答案为:HCl;Ba(OH)2;NaHCO3;Al2(SO4)3;AgNO3.
②B与C、D、E反应时,均有沉淀生成,且B过量时,D中的沉淀部分溶解,则B为氢氧化钡,D为硫酸铝;
③B与C、C与D反应生成的沉淀均可溶于A,则A为HCl,沉淀分别为碳酸钡、氢氧化铝;
④C的焰色反应呈黄色,往C中滴入少量A,有无色、无味的气体生成,则气体为二氧化碳,C中含Na元素,C为NaHCO3,
由上述分析可知A为HCl,B为Ba(OH)2,C为NaHCO3,D为Al2(SO4)3,E为AgNO3,
故答案为:HCl;Ba(OH)2;NaHCO3;Al2(SO4)3;AgNO3.
点评:本题考查物质的鉴别和检验,把握物质之间的反应及反应现象为解答的关键,注意白色沉淀的成分及性质,明确C为碳酸氢钠及氢氧化铝的两性即可解答,题目难度不大.

练习册系列答案
 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
已知0.1mol/L的碳酸氢钠溶液的pH为8.4,则下列说法正确的是( )
A、将该溶液加水稀释,
| ||
| B、加入少量KOH固体,钠离子和碳酸根离子浓度均增大 | ||
| C、c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | ||
| D、c(Na+)=c(HCO3- )+2c(CO32-)+c(H2CO3) |
以下四种溶液物质的量浓度均为0.01mol?L-1,下列说法正确的是( )
①NaHCO3②Na2CO3 ③CH3COOH ④CH3COONa.
①NaHCO3②Na2CO3 ③CH3COOH ④CH3COONa.
| A、①中各离子浓度为:c(Na+)>c(HCO3-)>c(OH-)>c(H+) | ||||||
B、②升高温度,
| ||||||
| C、③加入等体积的水稀释,电离平衡正向移动,c(H+)增大 | ||||||
| D、③和④等体积混合后溶液的pH<7,则c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
分子式为C6H12O2的酯经水解后,生成醇A和羧酸B,若A经氧化后生成B,则这种酯的结构可能有( )
| A、1种 | B、2种 |
| C、3种 | D、4种 E、5种 |
下列叙述正确的是( )
| A、测定相同温度下盐酸和醋酸溶液的pH,可证明盐酸是强酸、醋酸是弱酸 |
| B、改变温度能改变任何可逆反应的平衡状态 |
| C、离子反应的结果是自由移动的离子浓度减小 |
| D、Fe(OH)3胶体和饱和FeCl3溶液都呈红褐色,可通过丁达尔效应区分二者 |
2012年,将在京津冀、长三角、珠三角等重点区域以及直辖市和省会城市开展PM2.5(PM2.5是指大气中直径接近于2.5×10 -6m的颗粒物)和臭氧监测,下列有关说法正确的是( )
| A、PM2.5在空气中形成了气溶胶 |
| B、同温同压条件下,等质量的氧气和臭氧体积比为2:3 |
| C、16g臭氧中含有NA个原子 |
| D、1.00 mol臭氧中含有电子总数为18NA |
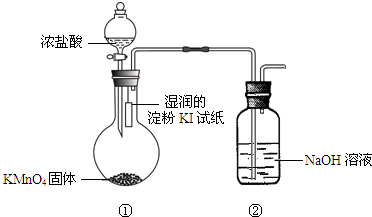 欲探究氯气与碘单质的氧化性强弱,某同学设计了如图装置(用浓盐酸和KMnO4固体反应制取氯气).
欲探究氯气与碘单质的氧化性强弱,某同学设计了如图装置(用浓盐酸和KMnO4固体反应制取氯气).