题目内容
【化学-选修3:物质结构与性质】
图甲所示为血红蛋白和肌红蛋白的活性部分--血红素的结构.
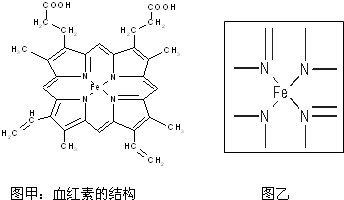
回答下列问题:
(1)血红素中含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是 ,写出基态Fe原子的价电子排布图 .
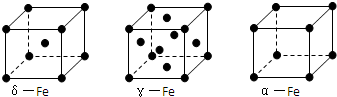
(2)血红素中两种N原子的杂化方式分别为 、 .在图乙的方框内用“→”标出Fe2+的配位键.(请考生自行在答题卡上先绘制图乙并在其上标出Fe2+的配位键)
(3)铁有δ、γ、α三种同素异形体,其对应的晶胞分别如下图所示,其中γ晶体晶胞中所含有的铁原子数为 ,δ、α两种晶胞中铁原子的配位数之比为 ;
若Fe的原子半径为r,则在δ-Fe晶胞中用r表示出这种堆积模型的空间利用率为 .(列式表示,不需化简)
与δ-Fe 具有相同堆积方式的金属还有 (填元素符号).
图甲所示为血红蛋白和肌红蛋白的活性部分--血红素的结构.

回答下列问题:
(1)血红素中含有C、H、O、N、Fe五种元素,C、H、N、O四种元素的电负性由小到大的顺序是
(2)血红素中两种N原子的杂化方式分别为
(3)铁有δ、γ、α三种同素异形体,其对应的晶胞分别如下图所示,其中γ晶体晶胞中所含有的铁原子数为
若Fe的原子半径为r,则在δ-Fe晶胞中用r表示出这种堆积模型的空间利用率为
与δ-Fe 具有相同堆积方式的金属还有

考点:元素电离能、电负性的含义及应用,原子核外电子排布,判断简单分子或离子的构型,晶胞的计算,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)根据元素周期表电负性的递变规律比较电负性强弱;结合能量最低原理、泡利不相容原理和洪特规则书写电子排布图;
(2)根据N原子的价电子排布式2s22p3,若N原子形成3个共价键,则氮原子周围还有一对孤对电子,即此时无配位键,该氮原子为sp3杂化,如NH3.若N原子形成4个共价键,则必有一个是配位键,若还存在双键(双键视为单键),则该氮原子为sp2杂化,如本题中的 ,若都为单键,则该氮原子为sp3杂化;
,若都为单键,则该氮原子为sp3杂化;
(3)利用均摊法计算晶胞的结构;
(2)根据N原子的价电子排布式2s22p3,若N原子形成3个共价键,则氮原子周围还有一对孤对电子,即此时无配位键,该氮原子为sp3杂化,如NH3.若N原子形成4个共价键,则必有一个是配位键,若还存在双键(双键视为单键),则该氮原子为sp2杂化,如本题中的
 ,若都为单键,则该氮原子为sp3杂化;
,若都为单键,则该氮原子为sp3杂化;(3)利用均摊法计算晶胞的结构;
解答:
解:(1)同周期元素从左到右元素的电负性逐渐增大,则有电负性C<N<O,H的电负性最小,
故有:H<C<N<O,基态Fe原子的核外价电子排布式为[Ar]3d64S2,则基态Fe原子的核外价电子排布图为 ;
;
故答案为:H<C<N<O; ;
;
(2)根据N原子的价电子排布式2s22p3,若N原子形成3个共价键,则氮原子周围还有一对孤对电子,即此时无配位键,该氮原子为sp3杂化,如NH3.若N原子形成4个共价键,则必有一个是配位键,若还存在双键(双键视为单键),则该氮原子为sp2杂化,如本题中的 ,若都为单键,则该氮原子为sp3杂化,如NH4+,
,若都为单键,则该氮原子为sp3杂化,如NH4+,
故答案为:sp2、sp3;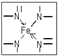 ;
;
(3)γ晶体晶胞中所含有的铁原子数为8×
+6×
=4,δ、α两种晶胞中铁原子的配位数分别为8、6,则配位数之比为8:6=4:3,δ晶胞为体心立方(堆积),体心立方中含有1+8×
=2;晶胞中铁原子的体积为:2×
×π×r3,体心立方中,体对角线上为三个铁原子相切,则体对角线为4r,晶胞边长为:
r=
r,晶胞体积为:(
r)3,空间利用率为:
×100%,与Na、K、具有相同堆积方式,
故答案为:4;4:3;
×100%;Na、K;
故有:H<C<N<O,基态Fe原子的核外价电子排布式为[Ar]3d64S2,则基态Fe原子的核外价电子排布图为
 ;
;故答案为:H<C<N<O;
 ;
;(2)根据N原子的价电子排布式2s22p3,若N原子形成3个共价键,则氮原子周围还有一对孤对电子,即此时无配位键,该氮原子为sp3杂化,如NH3.若N原子形成4个共价键,则必有一个是配位键,若还存在双键(双键视为单键),则该氮原子为sp2杂化,如本题中的
 ,若都为单键,则该氮原子为sp3杂化,如NH4+,
,若都为单键,则该氮原子为sp3杂化,如NH4+,故答案为:sp2、sp3;
 ;
;(3)γ晶体晶胞中所含有的铁原子数为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 8 |
| 4 |
| 3 |
| 4 | ||
|
4
| ||
| 3 |
4
| ||
| 3 |
2×
| ||||
(
|
故答案为:4;4:3;
2×
| ||||
(
|
点评:本题考查较为综合,涉及电负性、电子排布图、配位键、杂化方式以及晶胞的计算等问题,题目难度较大,易错点为(3).注意利用均摊法计算晶胞.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
第3周期元素的基态原子中,不可能出现d电子,主要依据是( )
| A、能量守恒原理 |
| B、泡利不相容原理 |
| C、洪特规则 |
| D、近似能级图中的顺序3d轨道能量比4s轨道高 |
下列有关原子核外电子排布的说法正确的是( )
| A、离核较近区域运动的电子能量较高 |
| B、M层最多容纳的电子数不超过8 |
| C、K层为最外电子层时最多只能容纳8个电子 |
| D、稀有气体元素的原子形成了稳定的电子层结构 |
下列判断中,正确的是( )
| A、可用NaOH溶液除去乙酸乙酯中混有的少量乙酸和乙醇 |
| B、可用水区别四种有机溶剂:苯、四氯化碳、己烯、无水乙醇 |
| C、淀粉水解的最终产物能与新制的氢氧化铜悬浊液反应生成砖红色的沉淀 |
| D、蒸馏“地沟油”可以获得甘油 |
在由水电离出的c(H+)=1×10-12 mol?L-1的溶液中,一定能大量共存的离子组是( )
| A、NH4+、Ba2+、NO3-、Cl- |
| B、Cl-、SO42-、Na+、K+ |
| C、SO42-、NO3-、Fe2+、Mg2+ |
| D、Na+、K+、ClO-、I- |
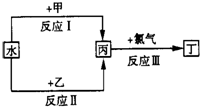
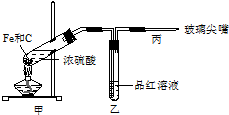 (1)下列仪器在使用前必须检查其是否漏水的是
(1)下列仪器在使用前必须检查其是否漏水的是