��Ŀ����
����Ŀ�����ᣨH2C2O4�����������һ�ִ�л�����������κͼ���������ˮ���������������ˮ����֪���ᾧ�壨H2C2O42H2O����ɫ��������ˮ���۵�Ϊ101����������ˮ��������170�����Ϸֽ⡣�Իش��������⣺

��1������ͬѧ������ͼ��ʾ��װ�ã�ͨ��ʵ�������ᾧ��ķֽ���װ��C�пɹ۲쵽������ð���ҳ���ʯ��ˮ����ǣ��ɴ˿�֪���ᾧ��ֽ�IJ�������______��
��2������ͬѧ��Ϊ���ᾧ��ֽ�IJ����к���CO��Ϊ������֤��ѡ�ü���ʵ���е�װ��A��B����ͼ��ʾ������װ���������ظ�ѡ�ã�����ʵ����
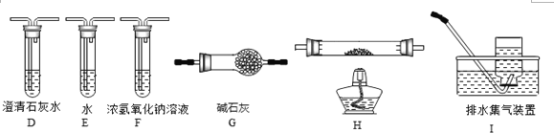
������ͬѧ��ʵ��װ���У��������ӵĺ���˳��Ϊ��A��B������ ����D��G������������D���ɣ�____________________
����֤�����ᾧ��ֽ��������CO��������____________________��___________________���ڶ���Dװ���г���ʯ��ˮ�������
���𰸡�CO2A��B����F�����ġ��ǡ���H�����ġ��������е�һ��Dװ���г���ʯ��ˮ�������H�к�ɫ��ĩ��Ϊ��ɫ
��������
��1�����ᾧ��ֽ�������ñ�ˮ���£�ˮ������ΪҺ�壬�ٰ�����ͨ�����ʯ��ˮ������ʯ��ˮ����ǣ���֤����ֽ���ﺬ��CO2���壻��2����Aװ���в��ᾧ��ֽ⣬ͨ��Bװ�ó�ȥˮ������������CO2��������������������Ӧ��2NaOH+CO2�TNa2CO3+H2O������������ͨ��Fװ�ó�ȥCO2���壬ͨ��D����CO2�Ѿ����ɾ�����Gװ�ø������壬Ȼ��ͨ��H�����ܣ�����ʯ��ˮ���飬����һ��ͨ��Dʯ��ˮ�������ǣ��ڶ���ͨ��ʯ��ˮ����ǣ�����H�еĹ����к�ɫ��Ϊ��ɫ��֤���ֽ�����к���CO���壮����CO�л�ԭ�ԣ�����װ��H��Ӧ����ʢ�е������Ǿ��������ԵĶ��ҿ�����CO��Ӧ�����ʣ���CuO�ȣ�����֤�����ᾧ��ֽ��������CO�������������е�һ��Dװ���г���ʯ��ˮ������ǣ�H�к�ɫ��ĩ��Ϊ��ɫ���ڶ���Dװ���г���ʯ��ˮ����ǣ�
��1�����Թ���ľ������ʱ��ʵ���������������ɣ����ܿ�������ð��������ʯ��ˮ����ǣ�֤����CO2�������ɣ���2����Ϊ��֤�ֽ��������CO����Ҫ�ų���֤�����ɵ�CO2��ʵ��ĸ��ţ�����Fװ������CO2���壬������Dװ��֤��CO2�Ѿ��������ٽ��CO�Ļ�ԭ�ԣ���D���ų������徭G�����ͨ��Hװ���м��ȵ�����ͭ������Dװ����֤CO������������CO2����֤��CO�Ĵ��ڣ�����ٽ���β������������װ�õ�����˳��ΪA��B��F��D��G��H��D��I��������Ӧ��������CO��ͨ���ų�CO2�ĸ��ź�������ʵ������ɹ۲쵽ͨHǰ��Dװ�ò������֤����CO2��H�к�ɫ��ĩ��Ϊ��ɫ֤���л�ԭ�����壬H�����Dװ���г���ʯ��ˮ�����֤����CO2���ɣ�

 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�����Ŀ�����淴ӦaA��g��+bB��s��cC��g��+dD��g���������������䣬C�����ʵ����������¶ȣ�T����ѹǿ��P����ϵ��ͼ��������ȷ���� ������ ��
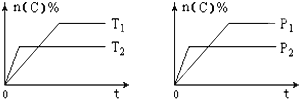
A. P1 > P2
B. �÷�Ӧ����H < 0
C. ��ѧ����ʽϵ��a��c+d
D. ʹ�ô�����C�����ʵ�����������
���𰸡�B
��������A.�ȹ���ƽ��ֵ������ͼ��֪��P2>P1����A����B. �ȹ���ƽ��ֵ������ͼ��֪��T2>T1�������¶�C�����ʵ���������С��˵�������¶�ƽ�������ƶ�����÷�ӦΪ���ȷ�Ӧ����H < 0����B��ȷ��C. ����ͼ��֪��P2>P1������ѹǿC�����ʵ���������С��˵������ѹǿƽ�������ƶ������淴Ӧ����Ϊ���������С�ķ������Ի�ѧ����ʽϵ��a��c+d����C����D. ʹ�ô�������ʹ��ѧƽ�ⷢ���ƶ�����C�����ʵ����������䣬��D����ѡB��
�����͡���ѡ��
��������
22
����Ŀ��25��ʱ��0.1 molL-1��Һ��pH���±��������й�˵����ȷ���� �� ��
��� | �� | �� | �� | �� |
��Һ | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A. ����ǿ����HF<H2CO3
B. �ٺ͢������ʾ�δˮ��
C. ��ˮ���������c(H+)����>��
D. ����Һ�У�c(HCO3-)+c(CO32-)+c(H2CO3)= c(Na+)

