题目内容
【题目】LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下:
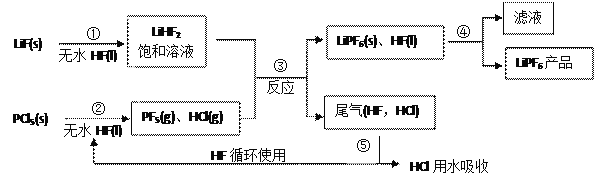
已知:HCl的沸点是—85.0℃,HF的沸点是19.5℃。
(1)第①步反应中无水HF的作用是____________、_____________。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的_______溶液冲洗。
(2)该流程需在无水条件下进行,第③步反应中PF5极易与水反应,其产物为两种酸,写出PF5与水反应的化学方程式:________________________________________。
(3)第④步分离采用的方法是_______;第⑤步分离尾气中HF、HCl采用的方法是_____________
【答案】反应物溶剂NaHCO3PF5 +4H2O==H3PO4+ 5HF过滤冷凝
【解析】
(1)根据流程可以看出,固体+液体→新物质+饱和溶液,所以无水HF的作用是反应物和溶剂;玻璃的主要成分中含有二氧化硅,能和HF发生反应;HF属于弱酸,可用弱碱性溶液来除去;(2)根据元素组成及其化合价可知,两种酸分别是H3PO4和HF;(3)分离液体和不溶于液体固体采用过滤分离,HF分子间含有氢键,沸点大于HCl,可采用冷凝法分离;
(1)根据题目中的流程,固体+液体→新物质+饱和溶液,无水HF的作用是反应物和溶剂;玻璃中含有二氧化硅,能和HF发生反应,化学方程式为SiO2+4HF═SiF4↑+2H2O;HF属于弱酸,可用弱碱性溶液来除去(比如2%的NaHCO3溶液);(2)根据信息“PF5极易水解,其产物为两种酸”,则根据元素组成及其化合价可知,两种酸分别是H3PO4和HF,反应的方程式为PF5+4H2O═H3PO4+5HF;(3)第④步分离的是固体(LiPF4(s))和液体(HF(l)),采用过滤的方法;分离尾气中HF、HCl,可以利用二者沸点的差异(HF分子之间存在氢键)进行分离,所以采用冷凝法。