题目内容
6.小刚、小红对一久置的NaOH白色粉末的成分进行探究.二位同学都作出以下的猜想:Ⅰ.①可能是NaOH; ②可能是Na2CO3; ③可能是NaOH与Na2CO3的混合物.做出②③猜想的依据是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示).
Ⅱ.为了验证①②③猜想,他们分别做了下面的实验.
(1)小刚取少量白色粉末于试管中,再滴加稀HCl,有气泡产生,由此可推出白色粉末中一定含有Na2CO3,可肯定猜想①(填序号)是错误的.
(2)为探究白色粉末是否含有NaOH,小红设计了如图实验方案:
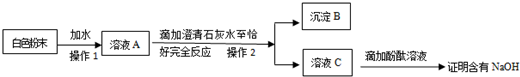
①沉淀B的化学式为CaCO3.
②在操作1中要用到玻璃棒,其作用是搅拌;在操作2中,除要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒外,还需补充的玻璃仪器是漏斗.
III.①小刚认为小红的这个方案有问题,理由是滴加澄清石灰水引入OH-,干扰NaOH的鉴别.
但只要将上述的澄清石灰水换成过量的CaCl2(填化学式)溶液,就可以证明粉末中还含有NaOH.
②小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定猜想③(填序号)是正确的.
③已知小刚取5.0g白色粉末进行试验,生成的沉淀B经过洗涤、干燥、称量,质量为3.0g,则白色固体中NaOH的质量分数为36.4%.(假设白色固体中不含其它杂质)如何判断沉淀B已经洗涤干净?取最后一次的洗涤液,滴入AgNO3溶液,观察是否有白色沉淀生成,若无则沉淀洗涤干净.
分析 Ⅰ.做出②③猜想的依据是氢氧化钠能与二氧化碳反应生成碳酸钠和水;
Ⅱ.(1)碳酸钠能与酸反应生成二氧化碳气体,根据实验现象可知白色粉末中一定含有碳酸钠;
(2)①碳酸钠与氢氧化钙反应生成碳酸钙;
②操作1加水溶解,玻璃棒的作用是搅拌使其充分溶解,操作2是将沉淀和溶液分开,为过滤,要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒,漏斗;
Ⅲ.①滴加澄清石灰水引入OH-,干扰NaOH的鉴别;将氢氧化钙换成氯化钙即可;
②加入过量的氯化钙溶液将碳酸根沉淀完全,得到沉淀B(碳酸钙),向滤液中滴加酚酞显红色,则证明粉末中含碳酸钠和氢氧化钠;
③沉淀B为碳酸钙,质量为3.0g,物质的量为$\frac{3.0g}{100g/mol}$=0.03mol,根据原子守恒可知白色固体中碳酸钠的物质的量为0.03mol,得出碳酸钠的质量,据此计算氢氧化钠的质量分数:$\frac{氢氧化钠的质量}{样品总质量}$×100%;取最后一次的洗涤液,滴入AgNO3溶液,观察是否有白色沉淀生成,若无则沉淀洗涤干净.
解答 解:Ⅰ.做出②③猜想的依据是氢氧化钠能与二氧化碳反应生成碳酸钠和水,反应方程式为:2NaOH+CO2=Na2CO3+H2O,
故答案为:2NaOH+CO2=Na2CO3+H2O;
Ⅱ.(1)碳酸钠能与酸反应生成二氧化碳气体,根据实验现象可知白色粉末中一定含有碳酸钠,说明猜想①是错误的,
故答案为:Na2CO3;①;
(2)①碳酸钠与氢氧化钙反应生成碳酸钙,则沉淀B是碳酸钙,
故答案为:CaCO3;
②操作1加水溶解,玻璃棒的作用是搅拌使其充分溶解,操作2是将沉淀和溶液分开,为过滤,要用到铁架台(带铁圈)、烧杯、滤纸、玻璃棒,漏斗,
故答案为:搅拌;漏斗;
Ⅲ.①当碳酸钠和氢氧化钠同时存在需要证明时,首先需要加入过量的氯化钙溶液检验并除去碳酸钠,滴加澄清石灰水虽能除碳酸根,但是引入OH-,干扰NaOH的鉴别,所以此方案不行,将氢氧化钙换成氯化钙即可,
故答案为:滴加澄清石灰水引入OH-,干扰NaOH的鉴别;CaCl2;
②加入过量的氯化钙溶液将碳酸根沉淀完全,得到沉淀B(碳酸钙),向滤液中滴加酚酞显红色,则证明粉末中含碳酸钠和氢氧化钠,说明猜想③正确,
故答案为:③;
③沉淀B为碳酸钙,质量为3.0g,物质的量为$\frac{3.0g}{100g/mol}$=0.03mol,根据原子守恒可知白色固体中碳酸钠的物质的量为0.03mol,则碳酸钠的质量为:0.03mol×106g/mol=3.18g,氢氧化钠的质量为:5.0g-3.18g=1.82g,氢氧化钠的质量分数为:$\frac{氢氧化钠的质量}{样品总质量}$×100%=$\frac{1.82g}{5.0g}$×100%=36.4%;取最后一次的洗涤液,滴入AgNO3溶液,观察是否有白色沉淀生成,若无则沉淀洗涤干净,
故答案为:36.4%;取最后一次的洗涤液,滴入AgNO3溶液,观察是否有白色沉淀生成,若无则沉淀洗涤干净.
点评 本题是探究物质的组成和测量物质的含量,通过提出问题、猜想与假设、实验设计,最后证实猜想,侧重考查学生对知识的迁移应用,难度中等.

| A. | 用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 将Fe3O4固体溶于HI溶液中:Fe3O4+8H+=2Fe3++Fe2++4H2O | |
| C. | 将氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向FeBr2溶液中通入少量的氯气:2Br-+Cl2=2Cl-+Br2 |
| A. | Ba2+和NO3- | B. | Na+和Cl- | C. | Ag+和SO42- | D. | Na+和NO3- |
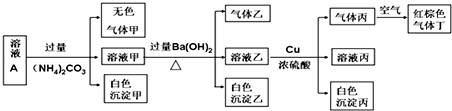
下列有关说法正确的是( )
| A. | 沉淀乙一定有BaCO3,可能有BaSO4 | |
| B. | 该溶液A中一定有NO3-、Al3+、SO42-、Cl- | |
| C. | 实验消耗Cu 14.4 g,则生成气体丙为3.36L | |
| D. | 生成的甲、乙、丙气体均为无色的易溶于水气体 |

| A. | 图二不是维生素C的结构简式 | |
| B. | 维生素C在碱性溶液中不能稳定存在 | |
| C. | 维生素C易发生起氧化及加成反应 | |
| D. | 维生素C易溶于水 |
| A. | 先向淀粉溶液中加入稀硫酸,再加入银氨溶液水浴加热,会有光亮的银镜出现 | |
| B. | 试管中先加入一定量浓硫酸,再依次加入适量冰醋酸、无水乙醇,然后加热制乙酸乙酯 | |
| C. | 配制银氨溶液时,将稀氨水慢慢滴入硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止 | |
| D. | 验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液 |