题目内容
1.将AgNO3、Na2SO4、BaCl2三种物质按物质的量为2:1:1的比例混合后溶于足量水中,最终溶液中大量存在的离子是( )| A. | Ba2+和NO3- | B. | Na+和Cl- | C. | Ag+和SO42- | D. | Na+和NO3- |
分析 AgNO3、Na2SO4、BaCl2三种物质按物质的量为2:1:1的比例,Ag+、Cl-以1:1结合生成沉淀,Ba2+、SO42-以1:1结合生成沉淀,以此来解答.
解答 解:AgNO3、Na2SO4、BaCl2三种物质按物质的量为2:1:1的比例,Ag+、Cl-以1:1结合生成沉淀,Ba2+、SO42-以1:1结合生成沉淀,则反应后溶液中溶质为硝酸钠,含离子为Na+和NO3-,
故选D.
点评 本题考查离子的共存,为高频考点,把握常见离子的性质及离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应的判断,题目难度不大.

练习册系列答案
相关题目
11.无水氯化铝在生产、生活中应用广泛.
(1)将氯化铝水溶液加热蒸干并灼烧得到的固体产物是Al2O3.
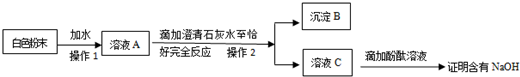
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如图:

已知:
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是防止后续步骤生成的AlCl3水解或增大反应物的接触面积,加快反应速率(写出两种).
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质的反应方程式是Fe2O3+3C$\frac{\underline{\;950℃\;}}{\;}$2Fe+3CO↑.
③已知:
Al2O3(s)+3C(s)═2Al(s)+3CO(g)△H1=+1344.1kJ•mol-1
2AlCl3(g)═2Al(s)+3Cl2(g)△H2=+1169.2kJ•mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g)△H=+174.9kJ/mol.
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为NaCl、NaClO、Na2CO3⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是除去FeCl3,提高AlCl3纯度.
⑥在Ⅰ至Ⅴ中涉及到氧化还原反应的有Ⅰ、Ⅱ、Ⅴ.
(1)将氯化铝水溶液加热蒸干并灼烧得到的固体产物是Al2O3.
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如图:

已知:
| 物质 | SiCl4 | AlCl3 | FeCl3[来 | FeCl2 |
| 沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质的反应方程式是Fe2O3+3C$\frac{\underline{\;950℃\;}}{\;}$2Fe+3CO↑.
③已知:
Al2O3(s)+3C(s)═2Al(s)+3CO(g)△H1=+1344.1kJ•mol-1
2AlCl3(g)═2Al(s)+3Cl2(g)△H2=+1169.2kJ•mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为Al2O3(s)+3C(s)+3Cl2(g)=2AlCl3(g)+3CO(g)△H=+174.9kJ/mol.
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为NaCl、NaClO、Na2CO3⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是除去FeCl3,提高AlCl3纯度.
⑥在Ⅰ至Ⅴ中涉及到氧化还原反应的有Ⅰ、Ⅱ、Ⅴ.
12.下列与有机物的结构、性质有关的说法正确的是( )
| A. | C5H12属于烷烃且有2种同分异构体 | |
| B. | 乙烯、氯乙烯、甲苯分子中的所有原子均共平面 | |
| C. | C4H10与Cl2在光照条件下反应,可生成4种一氯代烃 | |
| D. | 苯分子中不含碳碳双键,所以不能发生加成反应 |
9.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
| A. | 18gH2O含有的氢原子数目为NA | |
| B. | 标准状况下,22.4LCO2含有的分子数目为NA | |
| C. | 1L1mol•L-1K2SO4溶液中含有的钾离子数目为NA | |
| D. | 1molH2在O2中完全燃烧转移的电子数目为NA |
10.无机物氰酸铵(NH4OCN)受热可转化为有机物尿素[CO(NH2)2],这一反应的发现使人类踏上了有机合成的征程.下列关于这两种物质的说法中正确的是( )
| A. | 都属于铵盐 | B. | 都属于离子化合物 | ||
| C. | 互为同素异形体 | D. | 互为同分异构体 |
11.某溶液中仅含有一种溶质,若在该溶液中加入BaCl2溶液出现白色沉淀再加稀HNO3沉淀不消失,则该溶液不可能含有的溶质是( )
| A. | AgNO3 | B. | CuSO4 | C. | K2SO3 | D. | Na2CO3 |
 .
. .
.