题目内容
(1)在
O中,中子数为 ;该原子的原子结构示意图为 ,该原子与
O是 关系
(2)某金属氯化物MCl2 40.5克,含有0.60mol Cl-,则该氯化物的摩尔质量为 .
(3)化合物A是一种不稳定的物质,它的分子组成可用OxFy表示.10mLA气体能分解生成15mLO2和10mLF2(同温同压).则A的化学式是 ;
(4)配制50mL 0.2mol/L CuSO4溶液,需要CuSO4?5H2O g.
18 8 |
16 8 |
(2)某金属氯化物MCl2 40.5克,含有0.60mol Cl-,则该氯化物的摩尔质量为
(3)化合物A是一种不稳定的物质,它的分子组成可用OxFy表示.10mLA气体能分解生成15mLO2和10mLF2(同温同压).则A的化学式是
(4)配制50mL 0.2mol/L CuSO4溶液,需要CuSO4?5H2O
考点:物质的量的相关计算
专题:计算题
分析:(1)在
O中,质子数为8,质量数为18,原子核外有2个电子层,最外层电子数为6,与
O质子数相同,中子数不同;
(2)含有0.60mol Cl-,则n(MCl2)=0.30mol,根据M=
计算;
(3)10mLA气体能分解生成15mLO2和10mLF2(同温同压),则有2A=3O2+2F2,结合质量守恒计算;
(4)配制50mL 0.2mol/L CuSO4溶液,n(CuSO4?5H2O)=n(CuSO4)=0.2mol/L×0.05L=0.01mol,结合m=n×M计算.
18 8 |
16 8 |
(2)含有0.60mol Cl-,则n(MCl2)=0.30mol,根据M=
| m |
| n |
(3)10mLA气体能分解生成15mLO2和10mLF2(同温同压),则有2A=3O2+2F2,结合质量守恒计算;
(4)配制50mL 0.2mol/L CuSO4溶液,n(CuSO4?5H2O)=n(CuSO4)=0.2mol/L×0.05L=0.01mol,结合m=n×M计算.
解答:
解:(1)在
O中,质子数为8,质量数为18,中子数为18-8=10,原子核外有2个电子层,最外层电子数为6,则原子结构示意图为 ,与
,与
O质子数相同,中子数不同,互为同位素关系,
故答案为:10; ;同位素;
;同位素;
(2)含有0.60mol Cl-,则n(MCl2)=0.30mol,则M=
=
=135g/mol,故答案为:135g/mol;
(3)10mLA气体能分解生成15mLO2和10mLF2(同温同压),则有2A=3O2+2F2,由质量守恒定律可知A的化学式为O3F2,故答案为:O3F2;
(4)配制50mL 0.2mol/L CuSO4溶液,n(CuSO4?5H2O)=n(CuSO4)=0.2mol/L×0.05L=0.01mol,则需要CuSO4?5H2O 的质量为0.01mol×250g/mol=2.5g,
故答案为:2.5.
18 8 |
 ,与
,与16 8 |
故答案为:10;
 ;同位素;
;同位素;(2)含有0.60mol Cl-,则n(MCl2)=0.30mol,则M=
| m |
| n |
| 40.5g |
| 0.30ml |
(3)10mLA气体能分解生成15mLO2和10mLF2(同温同压),则有2A=3O2+2F2,由质量守恒定律可知A的化学式为O3F2,故答案为:O3F2;
(4)配制50mL 0.2mol/L CuSO4溶液,n(CuSO4?5H2O)=n(CuSO4)=0.2mol/L×0.05L=0.01mol,则需要CuSO4?5H2O 的质量为0.01mol×250g/mol=2.5g,
故答案为:2.5.
点评:本题考查较为综合,涉及原子结构、物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案
相关题目
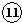
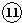 三种元素形成的气态氢化物最稳定的是
三种元素形成的气态氢化物最稳定的是