题目内容
11.某元素的单质为双原子分子,由于同位素的存在,其式量有2n-2、2n、2n+2三种(n为正整数),以下各值中肯定是该元素同位素质量数的是( )| A. | n-2 | B. | n | C. | n-1 | D. | 2n |
分析 设该元素的质量数种类为x,利用排列组合方法进行确定质量数种类,再结合相对分子质量计算其质量数.
解答 解:设该元素的质量数种类为x,且该元素的单质是双原子分子,其相对分子质量种类=Cx1+Cx2=x+$\frac{1}{2}$x(x-1)(x取正整数),解得x=2,所以其同位素有两种,双原子分子的相对分子质量有2n-2,2n,2n+2三种,相对分子质量的一半为该原子的相对原子质量,则其同位素的质量数为n-1 和n+1,
故选C.
点评 本题考查质量数和相对原子质量的关系、同位素的概念等知识点,会运用排列组合的方法解答,化繁为简,难度不大.

练习册系列答案
相关题目
6.将固体NH4I置于2L的密闭容器中,在一定温度下发生下列反应:①NH4I(S)?MH3(g)+HI(g)
②2HI(g)?H2(g)+I2(g)达到平衡时,n(H2)=1mol,n(HI)=8mol,则此温度下反应①的平衡常数为( )
②2HI(g)?H2(g)+I2(g)达到平衡时,n(H2)=1mol,n(HI)=8mol,则此温度下反应①的平衡常数为( )
| A. | 20 | B. | 16 | C. | 9 | D. | 25 |
16.下列离子在有关溶液中能大量共存的是( )
| A. | 澄清溶液中:AlO2-、SO42-、Na+、HCO3- | |
| B. | 在由水电离出的c(OH-)=10-13 mol•L-1的溶液中:I-、K+、Cl-、Ba2+ | |
| C. | 滴加甲基橙显红色的溶液:Fe2+、NH4+、SO42-、NO3- | |
| D. | c(H+)=c(OH-)的溶液:Fe3+、K+、Cl-、SO42- |
20.KMnO4可用于制备氧气,KMnO4属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
1.T℃时,将3molX和4molY充入1L密闭容器中,发生反应X(g)+3Y(g)?Z(g)+W(g),溶液中Y的物质的量浓度随时间变化如图中实线I所示,图中Ⅱ、Ⅲ表示仅改变某一反应条件时,Y的物质的量浓度随时间的变化,下列说法正确的是( )

| A. | 反应开始至a点时,v(X)=1mol•L-1•min-1 | |
| B. | 4min时,正反应速率:Ⅱ>Ⅰ | |
| C. | 曲线Ⅲ对应点的条件改变是减小压强 | |
| D. | T℃时,该反应的化学平衡常数为1 |


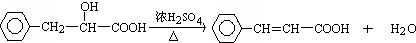 .
. .
. .
. 、
、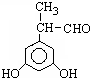 .
. (其中X、Y均部位H)
(其中X、Y均部位H)

 +(2n-1)H2O.
+(2n-1)H2O. .
.