��Ŀ����
19��ij�л���A��C4H6O5���㷺����������ˮ���ڣ�����ƻ�������ѡ����ϡ�ɽ�����࣬��һ�ֳ��õ�ʳƷ���Ӽ����û���������������ʣ���������25��ʱ������ƽ�ⳣ��K1=3.9��10-4��K2=5.5��10-6
������A+RCOOH����ROH��$\frac{\underline{\;Ũ����\;}}{��}$����ζ�IJ���
������1mol A$\stackrel{��������}{��}$��������1.5mol����
�������˴Ź������ױ���A��������5�ֲ�ͬ��ѧ��������ԭ�ӣ���A��صķ�Ӧ��ͼ���£�

��1�����ݻ�����A�����ʣ���A�Ľṹ���������ж���bc������ţ���
a���϶���̼̼˫�� b���������Ȼ�
c���϶����ǻ� d����-COOR������
��2��д��A��F�Ľṹ��ʽ��
A��HOOCCH��OH��CH2COOH��
F��HOOC-C��C-COOH��
��3��д�����з�Ӧ���ͣ�A-��B��ȥ��Ӧ��B-��E�ӳɷ�Ӧ��
��4��д�����з�Ӧ�ķ�Ӧ������E-��F�ڢٲ���ӦNaOH/����Һ����KOH/����Һ�������ȣ�
��5���ڴ��������£�B���Ҷ����ɷ������۷�Ӧ�����ɵĸ߷��ӻ������������첣���֣�д���÷�Ӧ�Ļ�ѧ����ʽ��nHOOC-CH�TCH-COOH+nHOCH2CH2OH$��_{��}^{����}$
 +��2n-1��H2O��
+��2n-1��H2O����6��д����A������ͬ�����ŵ�A��ͬ���칹��Ľṹ��ʽ��
 ��
��
���� A�в����Ͷ�=$\frac{4��2+2-6}{2}$=2��������ϢI֪��A�к��������Ȼ���A�ܺ����ᷢ��������Ӧ��������˵��A�к��д��ǻ���1molA�������Ʒ�Ӧ����1.5mol���������I��II֪����1�����ǻ��������Ȼ����˴Ź������ױ���A��������5�ֲ�ͬ��ѧ��������ԭ�ӣ���A�Ľṹ��ʽΪHOOCCH��OH��CH2COOH��
M�к���Clԭ�ӣ�M�ȼӳɺ�ȡ��Ȼ���ữ�õ�A����M�ṹ��ʽΪHOOCCCl=CHCOOH��A��Ũ���������������������·�Ӧ����B������B����ʽ֪��A������ȥ��Ӧ����B��B�ṹ��ʽΪHOOCCH=CHCOOH��B������NaOH��Ӧ����D��DΪNaOOCCH=CHCOONa��B����ȡ����Ӧ����E��EΪHOOCCHBrCHBrCOOH��E������ȥ��ӦȻ���ữ�õ�F������F����ʽ֪��FΪHOOC-C��C-COOH���ݴ˷������
��� �⣺A�в����Ͷ�=$\frac{4��2+2-6}{2}$=2��������ϢI֪��A�к��������Ȼ���A�ܺ����ᷢ��������Ӧ��������˵��A�к��д��ǻ���1molA�������Ʒ�Ӧ����1.5mol���������I��II֪����1�����ǻ��������Ȼ����˴Ź������ױ���A��������5�ֲ�ͬ��ѧ��������ԭ�ӣ���A�Ľṹ��ʽΪHOOCCH��OH��CH2COOH��
M�к���Clԭ�ӣ�M�ȼӳɺ�ȡ��Ȼ���ữ�õ�A����M�ṹ��ʽΪHOOCCCl=CHCOOH��A��Ũ���������������������·�Ӧ����B������B����ʽ֪��A������ȥ��Ӧ����B��B�ṹ��ʽΪHOOCCH=CHCOOH��B������NaOH��Ӧ����D��DΪNaOOCCH=CHCOONa��B����ȡ����Ӧ����E��EΪHOOCCHBrCHBrCOOH��E������ȥ��ӦȻ���ữ�õ�F������F����ʽ֪��FΪHOOC-C��C-COOH��
��1��A�в����Ͷ�=$\frac{4��2+2-6}{2}$=2��������ϢI֪��A�к��������Ȼ���A�ܺ����ᷢ��������Ӧ��������˵��A�к��д��ǻ���1molA�������Ʒ�Ӧ����1.5mol���������I��II֪����1�����ǻ��������Ȼ���
��ѡbc��
��2��ͨ�����Ϸ���֪��A��F�Ľṹ��ʽ�ֱ�Ϊ��HOOCCH��OH��CH2COOH��HOOC-C��C-COOH��
�ʴ�Ϊ��HOOCCH��OH��CH2COOH��HOOC-C��C-COOH��
��3��ͨ�����Ϸ���֪��A��B��B��E�ķ�Ӧ���ͷֱ�����ȥ��Ӧ���ӳɷ�Ӧ��
�ʴ�Ϊ����ȥ��Ӧ���ӳɷ�Ӧ��
��4��ͨ�����Ϸ���֪��E��F�ڢٲ���Ӧ����ȥ��Ӧ����Ӧ������NaOH/����Һ����KOH/����Һ�������ȣ�
�ʴ�Ϊ��NaOH/����Һ����KOH/����Һ�������ȣ�
��5��B�ṹ��ʽΪHOOCCH=CHCOOH���ڴ��������£�B���Ҷ����ɷ������۷�Ӧ�����ɵĸ߷��ӻ�����÷�Ӧ�Ļ�ѧ����ʽ��nHOOC-CH�TCH-COOH+nHOCH2CH2OH$��_{��}^{����}$ +��2n-1��H2O��
+��2n-1��H2O��
�ʴ�Ϊ��nHOOC-CH�TCH-COOH+nHOCH2CH2OH$��_{��}^{����}$ +��2n-1��H2O��
+��2n-1��H2O��
��6��A�Ľṹ��ʽΪHOOCCH��OH��CH2COOH��A��ͬ���칹����A������ͬ�����ţ�˵�����д��ǻ����Ȼ�������������A��ͬ���칹��Ľṹ��ʽ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ���������ȷ�ж�A�ṹ��ʽ�ǽⱾ��ؼ������ݷ�Ӧ����������ʽ�����ƶϣ�֪�������л���Ӧ���ͼ���Ӧ�������ѵ���ͬ���칹�������жϣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | Mg2+ | B�� | Fe3+ | C�� | Na+ | D�� | Na+ |
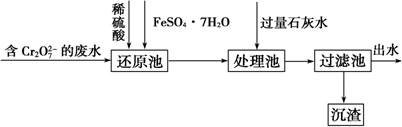
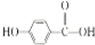
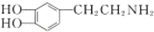 ��һ����Ҫ�������������ʣ�����������ϸ����������Ļ�ѧ���ʣ���Ӱ���˶�����Ļ�����ܣ���Ͱ�����D�������أ����������鷴Ӧ���پ�п���뻹ԭˮ���Ƶã��ϳɹ�����ͼ��ʾ��
��һ����Ҫ�������������ʣ�����������ϸ����������Ļ�ѧ���ʣ���Ӱ���˶�����Ļ�����ܣ���Ͱ�����D�������أ����������鷴Ӧ���پ�п���뻹ԭˮ���Ƶã��ϳɹ�����ͼ��ʾ��
 +H2$\stackrel{����}{��}$
+H2$\stackrel{����}{��}$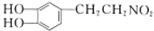 ��
�� ��
�� ��1��Ԫ��M�Ƕ�����Ԫ�أ��䳣�������ں�ˮ�У����ʱ���Ϊ��������������
��1��Ԫ��M�Ƕ�����Ԫ�أ��䳣�������ں�ˮ�У����ʱ���Ϊ��������������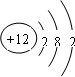 ��
��