题目内容
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合物加热有以下反应发生:2Cu2O+Cu2S
6Cu+SO2↑,填写下列空白:
①在该反应中,氧化剂是 .还原剂是 .
②氧化产物与还原产物的质量比是 .
| ||
①在该反应中,氧化剂是
②氧化产物与还原产物的质量比是
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应2Cu2O+Cu2S
6Cu+SO2↑中,Cu元素化合价由+1价变为0价,S元素化合价由-2价变为+4价,得电子化合价降低的反应物是氧化剂、失电子化合价升高的反应物是还原剂,氧化产物是SO2、还原产物是Cu.
| ||
解答:
解:①该反应2Cu2O+Cu2S
6Cu+SO2↑中,Cu元素化合价由+1价变为0价,S元素化合价由-2价变为+4价,所以氧化剂是Cu2O、Cu2S,还原剂是Cu2S,故答案为:Cu2O、Cu2S;Cu2S;
②氧化产物是SO2、还原产物是Cu,根据方程式知,氧化产物和还原产物的物质的量之比为1:6,故答案为:1:6.
| ||
②氧化产物是SO2、还原产物是Cu,根据方程式知,氧化产物和还原产物的物质的量之比为1:6,故答案为:1:6.
点评:本题考查了氧化还原反应,明确物质中元素化合价是解本题关键,再结合基本概念解答即可,注意Cu2O、Cu2S中Cu元素为+1价,为易错点.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
第三周期元素(不包括稀有气体),随着原子序数的递增,下列说法不正确的是( )
| A、最外层电子数逐渐增多 |
| B、原子半径逐渐减小 |
| C、简单离子半径逐渐减小 |
| D、元素的最高化合价逐渐增加 |
 实验室需要0.80mol?L-1 NaOH溶液475mL和0.40mol?L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题:
实验室需要0.80mol?L-1 NaOH溶液475mL和0.40mol?L-1硫酸500mL.根据这两种溶液的配制情况回答下列问题: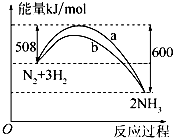 化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
化学反应过程中发生物质变化的同时,常常伴有能量的变化.这种能量的变化常以热量的形式表现出来,叫做反应热.由于反应的情况不同,反应热可以分为许多种,如燃烧热和中和热等.
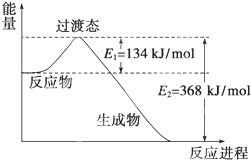 (1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:
(1)如图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: