��Ŀ����
�����仯�����ڹ�ũҵ������������������Ҫ���ã�

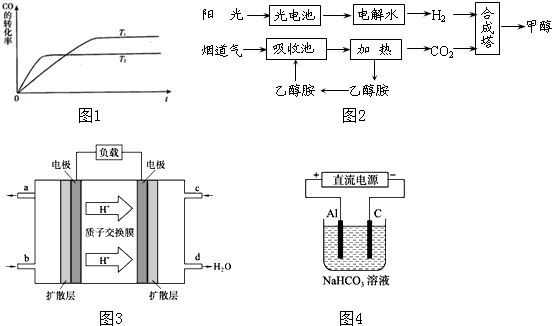
��1����T��ʱ����0.6mol H2��0.4mol N2�����ݻ�Ϊ2L���ܱ������У�ѹǿΪmPa��������Ӧ��3H2+N2?2NH3��H��0���������¶Ȳ��䣬ij��ȤС��ͬѧ��÷�Ӧ������������ѹǿ��ʱ��仯��ͼ1ʾ��8min�ڷ���NH3��ƽ����������Ϊ mol?L-1?min-1��
��2������T��ʱ����0.6mol H2��0.4mol N2����һ�ݻ��ɱ���ܱ������У�
�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ������ţ���
a��������N2��H2��NH3��Ũ��֮��Ϊl��3��2
b��3v����N2��=v����H2��
c��3v����H2��=2v����NH3��
d�����������ܶȱ��ֲ���
e�������������ƽ����Է�����������ʱ����仯
�߸������´ﵽƽ��ʱNH3������������⣨1��������NH3������������ ��������С�����䡱����
�۴ﵽƽ��ı�ijһ����ʹ��Ӧ���ʷ�������ͼ��ʾ�ı仯���ı������������ ��
a�������¶ȣ�ͬʱ��ѹ
b�������¶ȣ�ͬʱ��ѹ
c�������¶ȡ�ѹǿ���䣬����Ӧ��Ũ��
d�������¶ȡ�ѹǿ���䣬��С������Ũ��
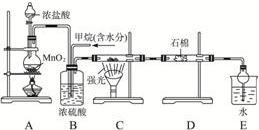
��3�����᳧��β�����е��������������ֱ���ŷŽ���Ⱦ�����������ܽ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ��
2NH3��g��+5NO2��g���T7NO��g��+3H2O��g����H=-akJ?mol-1
4NH3��g��+6NO��g���T5N2��g��+6H2O��g����H=-bkJ?mol-1
��NH3ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ�� ������״����NO��NO2�������40.32L��������ˮ��ȫ���գ�������״���µ���42.56L���û��������NO��NO2�����֮��Ϊ ��

��1����T��ʱ����0.6mol H2��0.4mol N2�����ݻ�Ϊ2L���ܱ������У�ѹǿΪmPa��������Ӧ��3H2+N2?2NH3��H��0���������¶Ȳ��䣬ij��ȤС��ͬѧ��÷�Ӧ������������ѹǿ��ʱ��仯��ͼ1ʾ��8min�ڷ���NH3��ƽ����������Ϊ
��2������T��ʱ����0.6mol H2��0.4mol N2����һ�ݻ��ɱ���ܱ������У�
�����и�����˵���÷�Ӧ�Ѵﵽƽ��״̬����
a��������N2��H2��NH3��Ũ��֮��Ϊl��3��2
b��3v����N2��=v����H2��
c��3v����H2��=2v����NH3��
d�����������ܶȱ��ֲ���
e�������������ƽ����Է�����������ʱ����仯
�߸������´ﵽƽ��ʱNH3������������⣨1��������NH3������������
�۴ﵽƽ��ı�ijһ����ʹ��Ӧ���ʷ�������ͼ��ʾ�ı仯���ı������������
a�������¶ȣ�ͬʱ��ѹ
b�������¶ȣ�ͬʱ��ѹ
c�������¶ȡ�ѹǿ���䣬����Ӧ��Ũ��
d�������¶ȡ�ѹǿ���䣬��С������Ũ��
��3�����᳧��β�����е��������������ֱ���ŷŽ���Ⱦ�����������ܽ��������ﻹԭΪ������ˮ���䷴Ӧ����Ϊ��
2NH3��g��+5NO2��g���T7NO��g��+3H2O��g����H=-akJ?mol-1
4NH3��g��+6NO��g���T5N2��g��+6H2O��g����H=-bkJ?mol-1
��NH3ֱ�ӽ�NO2��ԭΪN2���Ȼ�ѧ����ʽΪ��
���㣺��ѧƽ���ƶ�ԭ��,��Ӧ�Ⱥ��ʱ�,��Ӧ���ʵĶ�����ʾ����,��ѧƽ���Ӱ������,��ѧƽ��״̬���ж�,�йػ���ﷴӦ�ļ���
ר�⣺�����������������
��������1�����¶Ⱥ����һ���������£�ѹǿ֮�ȵ������ʵ���֮�ȣ�����ƽ��ʱ���������ʵ���Ϊ0.8����0.4+0.6��mol=0.8mol������N2+3H2?2NH3��n=2��֪�����ɵİ���Ϊ0.2mol���ٸ���v=
�������ʣ�
��2���ٺϳɰ���ӦΪ�����С�ķ��ȷ�Ӧ������ƽ��ʱ�����������淴Ӧ������ȣ���ɲ�����жϣ�
���ڢ����Ǻ����������������Ǻ�ѹ���������ݺϳɰ���ӦΪ�����С�Ŀ����жϣ�
����ͼ2���淴Ӧ���ʼ�С������Ӧ�������ݴ��жϣ�
��3�����ݸ�˹���ɿ���д���Ȼ�ѧ����ʽ�����ݵ��ӵ�ʧ�غ��Ԫ���غ���Լ��������ȣ�
| ��c |
| t |
��2���ٺϳɰ���ӦΪ�����С�ķ��ȷ�Ӧ������ƽ��ʱ�����������淴Ӧ������ȣ���ɲ�����жϣ�
���ڢ����Ǻ����������������Ǻ�ѹ���������ݺϳɰ���ӦΪ�����С�Ŀ����жϣ�
����ͼ2���淴Ӧ���ʼ�С������Ӧ�������ݴ��жϣ�
��3�����ݸ�˹���ɿ���д���Ȼ�ѧ����ʽ�����ݵ��ӵ�ʧ�غ��Ԫ���غ���Լ��������ȣ�
���
�⣺��1�����¶Ⱥ����һ���������£�ѹǿ֮�ȵ������ʵ���֮�ȣ�����ƽ��ʱ���������ʵ���Ϊ0.8����0.4+0.6��mol=0.8mol������N2+3H2?2NH3��n=2��֪�����ɵİ���Ϊ0.2mol���ٸ���v=
���������Ϊ
=0.0125mol?L-1?min-1���ʴ�Ϊ��0.0125��
��2���ٺϳɰ���ӦΪ�����С�ķ��ȷ�Ӧ������ƽ��ʱ�����������淴Ӧ������ȣ���ɲ�����жϣ�
a��������N2��H2��NH3��Ũ��֮������ʼ���йأ��뷴Ӧ�Ƿ���ƽ��״̬�أ���a����
b��3v����N2��=v����H2������Ӧ���ʵ��ڼ�����֮�ȣ�˵�����淴Ӧ������ȣ���b��ȷ��
c����Ӧ����ƽ��ʱ��2v����H2��=3v����NH3������c����
d����Ӧǰ��ѹǿ���䣬����仯�������غ㣬���Ի��������ܶȱ��ֲ���ʱ˵����Ӧ�Ѿ�����ƽ��״̬����d��ȷ��
e����Ӧǰ�������غ㣬���ʵ�����С�����Ե������������ƽ����Է�����������ʱ����仯ʱ��˵����Ӧ����ƽ��״̬����e��ȷ��
��ѡbde��
���ڢ����Ǻ����������������Ǻ�ѹ�������ﵽƽ��ʱѹǿ�Ȣ��еĴ���Ӧ�������С������ƽ���ƶ�ԭ������֪���еĴʴ�Ϊ�����
����ͼ2���淴Ӧ���ʼ�С������Ӧ�������������¶Ⱥ�ѹǿ�����䣬��Ϊ�¶Ⱥ�ѹǿ��ֻ��ʹ���淴Ӧ���ʶ������С�����Ըı��������ֻ�����ӷ�Ӧ��Ũ�ȣ����������������������Ӧ��Ũ�ȵ�ͬʱ������Ũ�ȼ�С����ѡc��
��3���ڷ�Ӧ��2NH3��g��+5NO2��g���T7NO��g��+3H2O��g����H=-akJ?mol-1�ͷ�Ӧ��4NH3��g��+6NO��g���T5N2��g��+6H2O��g����H=-bkJ?mol-1�и��ݸ�˹���ɣ������١�6+�ڡ�7��/5�ɵ��Ȼ�ѧ����ʽΪ6NO2��g��+8NH3��g���T7N2��g��+12H2O��g����H=-
kJ?mol-1��
�������40.32LΪ1.8mol������42.56LΪ1.9mol������Nԭ���غ����òμӷ�Ӧ�İ������ʵ�����
n��NH3��+1.8mol=1.9mol��2��n��NH3��=2mol��
����������ԭ��Ӧ�е�ʧ�����غ�����NO��NO2�����ʵ�����
��ΪNO�����ʵ���X��NO2�����ʵ���Ϊ��1.8mol-X����
2mol��3=Xmol��2+��1.8-X��mol��4��X=0.6mol����1.8mol-X��=1.2mol��
NO��NO2�����Ϊ0.6��1.2=1��2��
�ʴ�Ϊ6NO2��g��+8NH3��g���T7N2��g��+12H2O��g����H=-
kJ?mol-1��1��2����
| ��c |
| t |
| ||
| 8min |
��2���ٺϳɰ���ӦΪ�����С�ķ��ȷ�Ӧ������ƽ��ʱ�����������淴Ӧ������ȣ���ɲ�����жϣ�
a��������N2��H2��NH3��Ũ��֮������ʼ���йأ��뷴Ӧ�Ƿ���ƽ��״̬�أ���a����
b��3v����N2��=v����H2������Ӧ���ʵ��ڼ�����֮�ȣ�˵�����淴Ӧ������ȣ���b��ȷ��
c����Ӧ����ƽ��ʱ��2v����H2��=3v����NH3������c����
d����Ӧǰ��ѹǿ���䣬����仯�������غ㣬���Ի��������ܶȱ��ֲ���ʱ˵����Ӧ�Ѿ�����ƽ��״̬����d��ȷ��
e����Ӧǰ�������غ㣬���ʵ�����С�����Ե������������ƽ����Է�����������ʱ����仯ʱ��˵����Ӧ����ƽ��״̬����e��ȷ��
��ѡbde��
���ڢ����Ǻ����������������Ǻ�ѹ�������ﵽƽ��ʱѹǿ�Ȣ��еĴ���Ӧ�������С������ƽ���ƶ�ԭ������֪���еĴʴ�Ϊ�����
����ͼ2���淴Ӧ���ʼ�С������Ӧ�������������¶Ⱥ�ѹǿ�����䣬��Ϊ�¶Ⱥ�ѹǿ��ֻ��ʹ���淴Ӧ���ʶ������С�����Ըı��������ֻ�����ӷ�Ӧ��Ũ�ȣ����������������������Ӧ��Ũ�ȵ�ͬʱ������Ũ�ȼ�С����ѡc��
��3���ڷ�Ӧ��2NH3��g��+5NO2��g���T7NO��g��+3H2O��g����H=-akJ?mol-1�ͷ�Ӧ��4NH3��g��+6NO��g���T5N2��g��+6H2O��g����H=-bkJ?mol-1�и��ݸ�˹���ɣ������١�6+�ڡ�7��/5�ɵ��Ȼ�ѧ����ʽΪ6NO2��g��+8NH3��g���T7N2��g��+12H2O��g����H=-
| 6a+7b |
| 5 |
�������40.32LΪ1.8mol������42.56LΪ1.9mol������Nԭ���غ����òμӷ�Ӧ�İ������ʵ�����
n��NH3��+1.8mol=1.9mol��2��n��NH3��=2mol��
����������ԭ��Ӧ�е�ʧ�����غ�����NO��NO2�����ʵ�����
��ΪNO�����ʵ���X��NO2�����ʵ���Ϊ��1.8mol-X����
2mol��3=Xmol��2+��1.8-X��mol��4��X=0.6mol����1.8mol-X��=1.2mol��
NO��NO2�����Ϊ0.6��1.2=1��2��
�ʴ�Ϊ6NO2��g��+8NH3��g���T7N2��g��+12H2O��g����H=-
| 6a+7b |
| 5 |
������������Ҫ�����˻�ѧ��Ӧ���ʵļ��㡢ƽ��״̬���жϡ��Ȼ�ѧ��Ӧ����ʽ����д��������ԭ��Ӧ�ļ����֪ʶ�㣬�Ѷ��еȣ���һ�����ۺ��ԣ�

��ϰ��ϵ�д�
 ���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
���ɿ��õ�Ԫ������ĩר����100��ϵ�д�
�����Ŀ
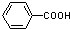 ���칹�干��7�֣�����3����
���칹�干��7�֣�����3����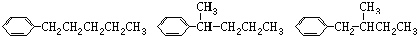 ����д������4�ֵĽṹ��ʽ��
����д������4�ֵĽṹ��ʽ��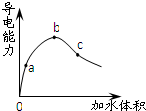 �����£���һ�����ı������ˮϡ�����У���Һ�ĵ��������仯��ͼ��ʾ��
�����£���һ�����ı������ˮϡ�����У���Һ�ĵ��������仯��ͼ��ʾ��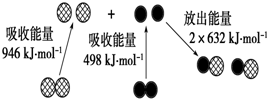 ��1����ѧ��Ӧ�е������仯�����ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ���£���ͼΪN2��g����O2��g������NO ��g�������е������仯��
��1����ѧ��Ӧ�е������仯�����ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ���£���ͼΪN2��g����O2��g������NO ��g�������е������仯��