题目内容
 [化学-物质结构与性质]
[化学-物质结构与性质]H、C、N、O、都属于自然界中常见非金属元素.
(1)O、C、N三种元素的第一电离能由小到大顺序是
(2)CO、N2的结构可表示为:两者的键能数据:(单位kJ/mol)
| A-B | A=B | A≡B | |
| CO | 357.7 | 798.9 | 1071.9 |
| N2 | 154.8 | 418.4 | 941.7 |
(3)乙二胺(H2N-CH2-CH2-NH2)和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是
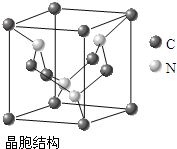
(4)C、N元素形成的新材料具有如右图所示结构,该晶体硬度将超过目前世界上最硬的金刚石,成为首屈一指的超硬新材料. 该物质的化学式为:
考点:晶胞的计算,元素电离能、电负性的含义及应用,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:(1)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素;根据价层电子对互斥理论确定其空间构型;
(2)根据断裂三键中的中的一个π键消耗的能量判断;
(3)乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,但三甲胺[N(CH3)3]分子之间不能形成氢键;
(4)利用均摊法确定其化学式.
(2)根据断裂三键中的中的一个π键消耗的能量判断;
(3)乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,但三甲胺[N(CH3)3]分子之间不能形成氢键;
(4)利用均摊法确定其化学式.
解答:
解:(1)同一周期元素的第一电离能随着原子序数的增大而呈增大的趋势,但第IIA族和第VA族元素的第一电离能大于相邻元素,所以C、N、O三种元素的第一电离能由大到小的顺序为:N>O>C;
NH4+中氮原子含有4个共价键,所以其轨道的杂化类是sp3杂化;
故答案为:N>O>C;sp3杂化;
(2)根据表中数据可知,断裂C≡O中的一个π键消耗的能量是1071.9kJ/mol-798.9kJ/mol=273kJ/mol,断裂N≡N中的一个π键消耗的能量是941.7kJ/mol-418.4kJ/mol=523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼.
故答案为:CO的第一个π键的键能为273kJ/mol,N2中的第一个π键的键能为523.3kJ/mol,所以CO的第一个键比N2更容易断裂;
(3)乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高.
故答案为:乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键;
(4)该晶胞中含有碳原子个数=8×
+4×
=3,N原子个数为4,所以其化学式为C3N4,故答案为:C3N4.
NH4+中氮原子含有4个共价键,所以其轨道的杂化类是sp3杂化;
故答案为:N>O>C;sp3杂化;
(2)根据表中数据可知,断裂C≡O中的一个π键消耗的能量是1071.9kJ/mol-798.9kJ/mol=273kJ/mol,断裂N≡N中的一个π键消耗的能量是941.7kJ/mol-418.4kJ/mol=523.3kJ/mol,断裂一个π键CO比N2更容易,所以CO更活泼.
故答案为:CO的第一个π键的键能为273kJ/mol,N2中的第一个π键的键能为523.3kJ/mol,所以CO的第一个键比N2更容易断裂;
(3)乙二胺(H2N-CH2-CH2-NH2)分子之间可以形成氢键,三甲胺[N(CH3)3]分子之间不能形成氢键,故乙二胺的沸点较高.
故答案为:乙二胺分子间可以形成氢键,三甲胺分子间不能形成氢键;
(4)该晶胞中含有碳原子个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
点评:本题考查物质与结构知识,涉及化学式的确定、氢键、电离能、原子杂化方式等知识点,这些都是高考热点,利用价层电子对互斥理论来确定微粒的空间构型及原子的杂化方式,难度中等.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
下列有关反应的离子方程式书写正确的是( )
A、亚硫酸氢铵溶液与含等物质的量的NaOH的溶液混合:N
| |||||||||||||||
B、氢氧化钡溶液与硫酸氢钠溶液反应至溶液恰好呈中性:Ba2++2H++SO42-+2OH-
| |||||||||||||||
C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-
| |||||||||||||||
D、向碳酸氢镁溶液中加入过量澄清石灰水:Mg2++2HC
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、遇Fe(CN)
| ||||
B、水电离出c(OH-)>10-5mol?L-1;Mg2+、Cl-、NO
| ||||
C、遇石蕊变红的溶液:Na+、NH
| ||||
D、与铝反应产生大量氢气的溶液:Ba2+、HCO
|
钛(Ti)被称为“生物金属”,由Ti0Ρ制取Ti的主要反应:
①Ti02+2Cl2+2C
TiCl4+2CO
②TICl4+2Mg
2MgCl2+Ti
下列说法不正确的是( )
①Ti02+2Cl2+2C
| ||
②TICl4+2Mg
| ||
下列说法不正确的是( )
| A、反应①②都是氧化还原反应 |
| B、反应②是置换反应 |
| C、反应①中Ti02:是氧化剂 |
| D、反应②中每生成1mol Ti转移4 mol电子 |
 近年来,化学工作者在CO2的应用研究上取得了一些重要成果.
近年来,化学工作者在CO2的应用研究上取得了一些重要成果. 含钡化合物在实验室和工业生产中都有广泛的用途.
含钡化合物在实验室和工业生产中都有广泛的用途.