题目内容
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、遇Fe(CN)
| ||||
B、水电离出c(OH-)>10-5mol?L-1;Mg2+、Cl-、NO
| ||||
C、遇石蕊变红的溶液:Na+、NH
| ||||
D、与铝反应产生大量氢气的溶液:Ba2+、HCO
|
考点:离子共存问题
专题:离子反应专题
分析:A.遇Fe(CN)
显蓝色的溶液,混有Fe2+;
B.水电离出c(OH-)>10-5mol?L-1,离子之间结合生成沉淀;
C.遇石蕊变红的溶液,溶液显酸性;
D.与铝反应产生大量氢气的溶液,为酸或强碱溶液.
3- 6 |
B.水电离出c(OH-)>10-5mol?L-1,离子之间结合生成沉淀;
C.遇石蕊变红的溶液,溶液显酸性;
D.与铝反应产生大量氢气的溶液,为酸或强碱溶液.
解答:
解:A.遇Fe(CN)
显蓝色的溶液,混有Fe2+,与ClO-发生氧化还原反应,不能共存,故A错误;
B.水电离出c(OH-)>10-5mol?L-1,Mg2+、OH-离子之间结合生成沉淀,不能共存,故B错误;
C.遇石蕊变红的溶液,溶液显酸性,该组离子之间不反应,能共存,故C正确;
D.与铝反应产生大量氢气的溶液,为酸或强碱溶液,HCO3-既能与酸反应又能与碱反应,则不能共存,故D错误;
故选C.
3- 6 |
B.水电离出c(OH-)>10-5mol?L-1,Mg2+、OH-离子之间结合生成沉淀,不能共存,故B错误;
C.遇石蕊变红的溶液,溶液显酸性,该组离子之间不反应,能共存,故C正确;
D.与铝反应产生大量氢气的溶液,为酸或强碱溶液,HCO3-既能与酸反应又能与碱反应,则不能共存,故D错误;
故选C.
点评:本题考查离子的共存,明确选项中的信息是解答的关键也是解答的难点,注意选项AB为解答的难点,题目难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
化工生产中常用MnS作沉淀剂除去Ksp工业废水中的Cu2+:Cu2+(aq)+MnS(s)?CuS(s)+Mn2+(aq),下列说法错误的是( )
| A、MnS的Ksp比CuS的Ksp大 | ||
| B、该反应达到平衡时c(Mn2+)=c(Cu2+) | ||
| C、往平衡体系中加入少量CuSO4固体后,C(Mn2+)变大 | ||
D、该反应的平衡常数K=
|
下列说法或表述正确的是( )
| A、由水电离产生的c(H+)=1×10-2mol?L-1溶液中,可能存在:CO32-、NH4+、Cl-,Na+ |
| B、某醋酸稀溶液的pH=a,将此溶液稀释1倍后,溶液的pH=b,则a>b |
| C、Ba(OH)2溶液中加人过量的Al2(SO4)3溶液,其离子方程式为:3Ba2++60H-+2Al3++3SO42-=3BaS04↓+2Al(0H)3↓ |
| D、物质的量浓度均为1mol?L-1的NaCl和MgCl2混合液中,含有Cl-的数目为3NA(NA表示阿伏加德罗常数的值) |
设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、一定温度下,pH=6的纯水中含有的 OH-数为 10-6 NA |
| B、1 L 0.1 mol?L-1的醋酸溶液中含有的离子和分子的总数为 0.1 NA |
| C、1.2 g NaHSO4晶体中含有的阳离子和阴离子的总数为 0.03 NA |
| D、常温常压下,56 g乙烯和丙烯的混合气中含有的碳原子数为 4 NA |
 已知氧化还原反应:2KMn04+10FeS04+8H2SO4?2MnS04+5Fe2(S04)3+K2S04+8H2O.控制适当的条件,将上述反应设计成如图所示的原电池.下列判断不正确的是( )
已知氧化还原反应:2KMn04+10FeS04+8H2SO4?2MnS04+5Fe2(S04)3+K2S04+8H2O.控制适当的条件,将上述反应设计成如图所示的原电池.下列判断不正确的是( )| A、随着反应进行,甲中颜色逐渐变浅,乙中颜色逐渐变深 |
| B、反应开始时,甲中石墨电极上的电极反应式为Mn04-+8H++5e-═Mn2++4H20 |
| C、反应开始时,乙中石墨电极上发生还原反应 |
| D、电流计读数为零时,反应达到化学平衡状态 |
下列有关化学用语表示正确的是( )
A、CO2分子比例模型: | ||
B、S2-的结构示意图: | ||
C、质子数为53,中子数为78的碘原子:
| ||
D、过氧化氢的电子式: |

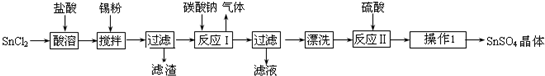
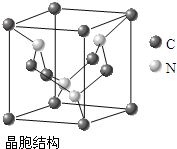 [化学-物质结构与性质]
[化学-物质结构与性质]