题目内容
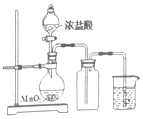
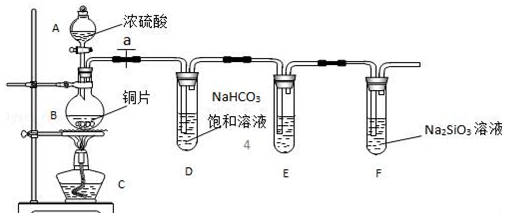
3.ClO2是一种易溶于水而难溶于有机溶剂的气体,可作为一种广谱型的消毒剂.实验室制备ClO2的原理是用亚氯酸钠固体(NaClO2)与纯净的氯气反应:2NaClO2+Cl2═2ClO2+2NaCl如图是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略).其中E中盛有CCl4液体,用于除去ClO2中的未反应的Cl2.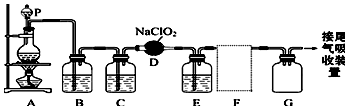
(1)写出装置A中烧瓶内发生反应的化学方程式MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2++Cl2↑+2H2O.
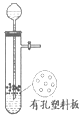
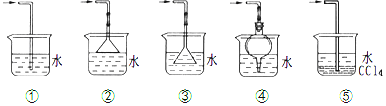
(2)F处应选用的收集装置是②(填序号),其中与E装置导管相连的导管口是d(填接口字母).

(3)以下是尾气吸收装置,能用于吸收多余ClO2气体,并能防止倒吸的装置的是②④⑤.
分析 由题目中所给信息和实验装置图可知:本实验首先用浓盐酸和MnO2在加热条件下反应制备Cl2,反应的方程式为MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2++Cl2↑+2H2O,制得的氯气中混有氯化氢气体和水蒸气,经饱和食盐水除杂氯化氢气体、浓硫酸干燥后在D中亚氯酸钠固体反应生成ClO2,由于Cl2易溶于CCl4液体,E用于除去ClO2中的未反应的Cl2,最后用向上排空法收集,据此分析.
解答 解:(1)A装置为浓盐酸和MnO2在加热条件下反应制备Cl2,反应的方程式为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2++Cl2↑+2H2O;
故答案为:MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2++Cl2↑+2H2O;
(2)ClO2是一种易溶于水的气体,且密度比空气大,应用向上排空气法收集,且进行尾气处理,故用双孔橡皮塞;
故答案为:②; d;
(3)ClO2是一种易溶于水的气体,尾气吸收时要防止倒吸,导气管不能插入到液面以下,②④⑤符合;
故答案为:②④⑤.
点评 本题考查气体的制备、除杂、收集等实验操作,题目难度不大,学习中注意把握化学实验基本操作,做该类题目时把握实验目的和实验原理是解答题目的关键.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
8. 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.
如图表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A. | 25℃时,相同浓度的NaHCO3溶液的碱性大于NaClO溶液 | |
| B. | 图象中a点的导电能力小于c点 | |
| C. | 图象 I代表CH3COOH溶液的稀释 | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
9.鉴别溶液中Cl-、Br-、I-,可以使用的试剂为( )
| A. | 碘水、淀粉溶液 | B. | 溴水、四氯化碳 | ||
| C. | 盐酸、氯化钡溶液 | D. | 硝酸银溶液、稀硝酸 |
13.实现下列变化时,需克服相同类型作用力的是( )
| A. | 水晶和干冰的熔化 | B. | 食盐和冰醋酸熔化 | ||
| C. | 液溴和金刚石的气化 | D. | 纯碱和烧碱的熔化 |
12.下列离子方程式,书写正确的一项是( )
| A. | 向氯化铁溶液中加入Cu单质:Cu+Fe3+═Fe2++Cu2+ | |
| B. | 向盐酸中加入Cu:Cu+2H+═Cu2++H2↑ | |
| C. | 向NaOH溶液中加入硫酸:OH-+H+═H2O | |
| D. | 向CuSO4溶液中加入钠:2Na+Cu2+═2Na++Cu |
13.现有NaCl、FeC12、FeCl3、MgCl2、AlCl3五种溶液,只用一种试剂就可以鉴别它们,这种试剂是( )
| A. | 盐酸 | B. | NaOH溶液 | C. | 氨水 | D. | KSCN溶液 |