题目内容
下列叙述正确的是( )
| A、化学键存在所有物质中 |
| B、化学键的断裂和形成是化学反应能量变化的主要原因 |
| C、只要有能量变化,则一定发生了化学反应 |
| D、当反应物的总能量低于生成物的总能量时,该反应放出能量 |
考点:化学键,反应热和焓变
专题:
分析:A.稀有气体中不存在化学键;
B.化学反应的实质为化学键的断裂和形成,断裂吸收能量,形成释放能量;
C.物理变化中也有能量变化;
D.当反应物的总能量低于生成物的总能量时,该反应发生时需要吸收能量.
B.化学反应的实质为化学键的断裂和形成,断裂吸收能量,形成释放能量;
C.物理变化中也有能量变化;
D.当反应物的总能量低于生成物的总能量时,该反应发生时需要吸收能量.
解答:
解:A.稀有气体为单原子构成的分子,不存在化学键,故A错误;
B.化学反应的实质为化学键的断裂和形成,断裂吸收能量,形成释放能量,则化学键的断裂和形成是化学反应能量变化的主要原因,故B正确;
C.物理变化中也有能量变化,如浓硫酸稀释,物质三态变化等,不发生化学变化,故C错误;
D.当反应物的总能量低于生成物的总能量时,该反应发生时需要吸收能量,即该反应为吸热反应,故D错误;
故选B.
B.化学反应的实质为化学键的断裂和形成,断裂吸收能量,形成释放能量,则化学键的断裂和形成是化学反应能量变化的主要原因,故B正确;
C.物理变化中也有能量变化,如浓硫酸稀释,物质三态变化等,不发生化学变化,故C错误;
D.当反应物的总能量低于生成物的总能量时,该反应发生时需要吸收能量,即该反应为吸热反应,故D错误;
故选B.
点评:本题考查化学键及反应中能量变化,为高频考点,把握化学键的形成及化学反应的实质为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
11H、21H是氢元素的两种核素,168O、188O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法中正确的是( )
| A、168O、188O的核外电子排布不相同 |
| B、通过化学反应,可以实现168O和188O之间的相互转化 |
| C、18g 11H2168O中所含电子数为10NA |
| D、18g21H2168O中含中子数为10NA |
有甲、乙、丙、丁四种元素,其价电子数依次为1、2、6、7,其电子层数依次减少.已知丁离子的电子层结构与氩原子相同,甲和乙的次外层各有8个电子,丙的次外层有18个电子.据此下列判断错误的是( )
| A、第一电离能由大到小的顺序是:丁>丙>乙>甲 |
| B、原子半径由大到小的顺序是:甲>乙>丙>丁 |
| C、金属性由强到弱的顺序是:甲>乙>丙>丁 |
| D、电负性由小到大的顺序是:乙<丙<丁<甲 |
 根据下列要求回答相关问题:
根据下列要求回答相关问题:

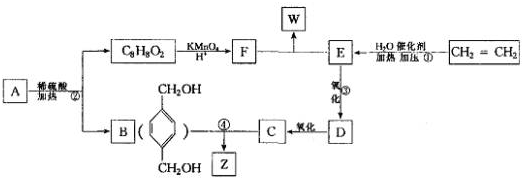
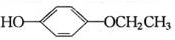 ,
,