题目内容
物质在反应中可表现氧化性、还原性、酸性、碱性等,下面方程式中划线的物质,能在同一反应中同时表现上述两种或两种以上性质的有( )
①3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
③8NH3+3Cl2=6NH4Cl+N2
④2Na2O2+2H2O=4NaOH+O2↑
①3FeO+10HNO3=3Fe(NO3)3+NO↑+5H2O
②C+2H2SO4(浓)=CO2↑+2SO2↑+2H2O
③8NH3+3Cl2=6NH4Cl+N2
④2Na2O2+2H2O=4NaOH+O2↑
| A、①②③ | B、①③④ |
| C、②③④ | D、全部 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:①生成NO体现硝酸的氧化性,生成硝酸铁体现硝酸的酸性;
②只体现硫酸的氧化性;
③生成氮气体现氨气的还原性,生成氯化铵体现碱性;
④过氧化钠中O元素的化合价既升高又降低.
②只体现硫酸的氧化性;
③生成氮气体现氨气的还原性,生成氯化铵体现碱性;
④过氧化钠中O元素的化合价既升高又降低.
解答:
解:①生成NO体现硝酸的氧化性性,生成硝酸铁体现硝酸的酸性;
②只体现硫酸的氧化性;
③生成氮气体现氨气的还原性,生成氯化铵体现碱性;
④过氧化钠中O元素的化合价既升高又降低,体现氧化性和还原性,
能在同一反应中同时表现上述两种或两种以上性质的有①③④,
故选B.
②只体现硫酸的氧化性;
③生成氮气体现氨气的还原性,生成氯化铵体现碱性;
④过氧化钠中O元素的化合价既升高又降低,体现氧化性和还原性,
能在同一反应中同时表现上述两种或两种以上性质的有①③④,
故选B.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析及应用能力的考查,注意从化合价角度分析氧化性、还原性,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知乙酸(HA)的酸性比甲酸(HB)弱,在物质的量浓度均为0.1mol?L-1的NaA和NaB混合溶液中,下列排序正确的是( )
| A、c(OH-)>c(HA)>c(HB)>c(H+) |
| B、c(OH-)>c(A-)>c(B-)>c(H+) |
| C、c(OH-)>c(B-)>c(A-)>c(H+) |
| D、c(OH-)>c(HB)>c(HA)>c(H+) |
利尿酸是奥运会禁止使用的兴奋剂之一,其结构简式如图.下列有关利尿酸的说法中正确的是( )

| A、分子式是C13H14O4Cl2 |
| B、1mol利尿酸最多能与5mol H2发生加成反应 |
| C、-定条件下能发生加聚、缩聚反应 |
| D、分子中所有碳原子不可能共平面 |
某原电池装置如图所示,下列有关叙述中,不正确的是( )
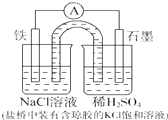

| A、Fe作负极,发生氧化反应 |
| B、盐桥的作用是平衡电荷,构成闭合回路 |
| C、工作一段时间后,NaCl溶液中c(Cl-)不变 |
| D、正极反应:2H++2e-=H2↑ |