题目内容
浓度是影响反应能否发生的因素之一.下列说法符合事实的是( )
| A、常温下,铝片可以溶解于足量浓硫酸,也可溶解于足量稀硫酸 |
| B、常温下,铜片与浓硝酸反应,不与稀硝酸反应 |
| C、常温下,浓的氢氧化钠溶液和极稀的氢氧化钠溶液均能溶解Al(OH)3 |
| D、常温下,锌与浓硫酸和稀硫酸都能反应,但生成的气体不同 |
考点:化学反应速率的影响因素,硝酸的化学性质,浓硫酸的性质
专题:化学反应速率专题,元素及其化合物
分析:A.常温下,铝片与浓硫酸发生钝化;
B.硝酸具有强氧化性;
C.极稀的氢氧化钠溶液,碱性较弱;
D.锌与浓硫酸和稀硫酸都反应,分别生成二氧化硫、氢气.
B.硝酸具有强氧化性;
C.极稀的氢氧化钠溶液,碱性较弱;
D.锌与浓硫酸和稀硫酸都反应,分别生成二氧化硫、氢气.
解答:
解:A.常温下,铝片与浓硫酸发生钝化,则铝片不能溶解于足量浓硫酸,但可溶解于足量稀硫酸,故A错误;
B.硝酸具有强氧化性,常温下,铜片与浓硝酸、稀硝酸均反应,故B错误;
C.极稀的氢氧化钠溶液,碱性较弱,不能溶解Al(OH)3,故C错误;
D.锌与浓硫酸和稀硫酸都反应,分别生成二氧化硫、氢气,故D正确;
故选D.
B.硝酸具有强氧化性,常温下,铜片与浓硝酸、稀硝酸均反应,故B错误;
C.极稀的氢氧化钠溶液,碱性较弱,不能溶解Al(OH)3,故C错误;
D.锌与浓硫酸和稀硫酸都反应,分别生成二氧化硫、氢气,故D正确;
故选D.
点评:本题考查物质的性质,综合考查元素化合物知识,为高频考点,把握浓硫酸、硝酸、氢氧化铝、盐酸的性质及氧化还原反应原理为解答的关键,题目难度不大.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案
相关题目
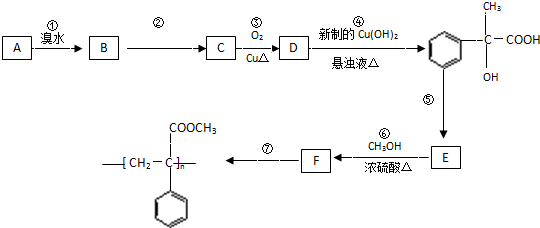
 2008年夏季奥运会即将在我国举行,我国支持“绿色奥运、科技奥运、人文奥运”,人文奥运的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图,有关该物质的说法正确的是( )
2008年夏季奥运会即将在我国举行,我国支持“绿色奥运、科技奥运、人文奥运”,人文奥运的一个重要体现是坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图,有关该物质的说法正确的是( )| A、属于芳香烃 |
| B、属于高分子化合物 |
| C、属于苯酚的同系物 |
| D、与溴水可发生加成反应和取代反应 |
下列物质与常用危险化学品的类别不对应的是( )
| A、H2SO4、NaOH--腐蚀品 |
| B、CH4、H2--易燃液体 |
| C、白磷--易燃固体 |
| D、KMnO4、H2O2--氧化剂 |
某二元酸H2A在水中发生电离:H2A=H++HA-(完全电离),HA-?H++A2-.下列叙述中一定不正确的是( )
| A、在NaHA溶液中:c(Na+)>c(HA-)>c(OH-)>c(H+) |
| B、在Na2A溶液中:c(Na+)>c(A2-)>c(OH-)>c(H+) |
| C、在NaHA溶液中:c(H+)=c(A2-)+c(OH-) |
| D、在H2A溶液中:c(H+)=c(HA-)+c(OH-)+2c(A2-) |
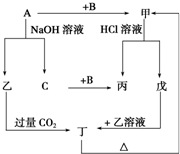 由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料.请回答:
由短周期元素组成的单质A、B、C和甲、乙、丙、丁、戊五种化合物有如图所示的转换关系,甲是工业上制取A的主要原料.请回答: