题目内容
A、B、C是元素周期表中前18号元素间组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图的关系:

试填写下列空白:
(1)A、B、C的化学式分别为 、 、 .
(2)单质甲与化合物B反应的离子方程式为 .
(3)在A、B、C这三种化合物中,必定含有的元素是 (用“甲”、“乙”或“丙”表示).

试填写下列空白:
(1)A、B、C的化学式分别为
(2)单质甲与化合物B反应的离子方程式为
(3)在A、B、C这三种化合物中,必定含有的元素是
考点:无机物的推断
专题:推断题
分析:化合物A和化合物B反应生成单质乙和化合物C,常见的反应有:①2Na2O2+2CO2=2Na2CO3+O2、②2Na2O2+2H2O=4NaOH+O2↑、③2H2O2
2H2O+O2↑等,A、B、C是元素周期表中前18号元素间组成的三种常见化合物,则反应③可排除;
根据①、②单质乙可能为氧气;若A为二氧化碳,则B为二氧化碳,C为碳酸钠,单质甲与B反应生成C,而氧气不能与二氧化碳反应生成碳酸钠,依次对反应①、②进行分析讨论得出乙是氧气、B是H2O、C是NaOH、A是Na2O2,据此进行解答各题.
| ||
根据①、②单质乙可能为氧气;若A为二氧化碳,则B为二氧化碳,C为碳酸钠,单质甲与B反应生成C,而氧气不能与二氧化碳反应生成碳酸钠,依次对反应①、②进行分析讨论得出乙是氧气、B是H2O、C是NaOH、A是Na2O2,据此进行解答各题.
解答:
解:(1)化合物A和B反应生成单质乙和化合物C,两种化合物生成单质和化合物,且是短周期元素形成的化合物,则可能的反应有:①2Na2O2+2CO2=2Na2CO3+O2、②2Na2O2+2H2O=4NaOH+O2↑,再根据甲和乙生成A、甲和B生成C和B、丙和乙生成B、甲和B生成丙和C可知,A为Na2O2、B为H2O、乙为O2、C为NaOH,
故答案为:Na2O2;H2O;NaOH;
(2)单质甲为钠,化合物B为H2O,二者反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(3)在A、B、C三种化合物中,乙和丙生成B,则B中含有乙和丙;甲和乙生成A,则A中含有甲和乙;甲和B(含有乙和丙)生成丙和C,根据原子守恒,则C中一定含有甲和乙,所以A、B、C中都含有的元素为乙,
故答案为:乙.
故答案为:Na2O2;H2O;NaOH;
(2)单质甲为钠,化合物B为H2O,二者反应的离子方程式为:2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(3)在A、B、C三种化合物中,乙和丙生成B,则B中含有乙和丙;甲和乙生成A,则A中含有甲和乙;甲和B(含有乙和丙)生成丙和C,根据原子守恒,则C中一定含有甲和乙,所以A、B、C中都含有的元素为乙,
故答案为:乙.
点评:本题考查了无机推断,侧重钠及其化合物性质的考查,题目难度较大,依据化学反应类型,结合物质性质的转化关系分析判断是解题关键,试题培养了学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
下列解释事实的方程式不正确的是( )
| A、测0.1 mol/L的氨水的pH为11:NH3?H2O?NH4++OH- | ||||
| B、将Na块放入水中,产生气体:2Na+2H2O═2OH-+2Na++H2↑ | ||||
| C、Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | ||||
D、用CuCl2溶液做导电性实验,灯泡发光:CuCl2
|
某分子式为C10H20O2的酯,在一定条件下可发生如图的转化过程:则符合上述条件的酯的结构可有( )
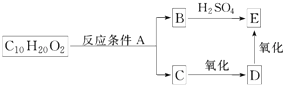

| A、2种 | B、4种 | C、6种 | D、8种 |
在标准状况下,将V L A气体(摩尔质量M g/mol)溶于100ml水中(A与水不反应),所得A的水溶液密度为ρ g/cm3,则此溶液的物质的量浓度(mol/L)为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
化学中常用图象直观地描述化学反应的进程或结果.下列对图象的叙述正确的是( )
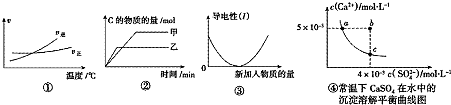

| A、根据图①可判断可逆反应A2(g)+3B2(g)?2AB2(g),正反应是吸热反应 |
| B、图②可表示压强对反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
| C、图③可表示乙酸溶液中通人氨气至过量的过程中溶液导电性的变化 |
| D、根据图④可知,a点对应的KSP等于c点对应的KSP |
 (1)已知298K时,1mol CH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.3kJ.写出该反应的热化学方程式:
(1)已知298K时,1mol CH4在氧气中完全燃烧生成二氧化碳和液态水,放出热量890.3kJ.写出该反应的热化学方程式: