题目内容
9.葡萄酒中抗氧化剂的残留量是以游离SO2计算的,我国国家标准(CB2760-2011)规定葡萄酒中SO2残留量≤0.25g•L-1.为测定某葡萄酒中SO2含量设定方案如下:
用图一装置(夹持装置略)蒸馏并收集馏分SO2,实验时B中加入100.00mL葡萄酒样品和适量盐酸,加热使SO2全部逸出,在C中收集馏分.
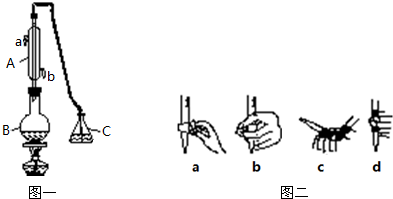
(1)若C中盛装H2O2溶液,SO2与其完全反应,除去C中过量的H2O2,然后用0.04000mol•L-1NaOH标准溶液进行滴定,滴定前排气泡时,应选择图二中的c.
滴定至终点消耗NaOH溶液25.00mL,据此计算葡萄酒中SO2含量为0.32g•L-1.
(2)由于蒸馏时盐酸易挥发,该测定结果比实际值偏高(填“偏高”、“偏低”或“无影响”),因此改进实验方案时可将盐酸改为稀硫酸,或者采取以下措施:
Ⅰ.在之前实验基础上,通过测定C中Cl-含量进而计算SO2实际含量:除去C中的SO42-,然后用AgNO3标准溶液滴定Cl-,K2CrO4溶液为指示剂.
已知:常温下Ksp(AgCl)=2×10-10,Ksp(Ag2CrO4)=1.12×10-12,Ag2CrO4为砖红色.滴定过程中,当观察到出现淡红色沉淀且不再消失时停止滴定,若此时Cl-恰好沉淀完全即溶液中残余c(Cl-)=1.0×10-5 mol•L-1,则此时溶液中的c(CrO42-)=2.8×10-3mol•L-1.
Ⅱ.将图一装置C中盛装的液体改为H2O,且馏分无挥发,改用0.01000mol•L-1标准I2溶液滴定,反应的化学方程式为SO2+I2+2H2O═H2SO4+2HI,可选择淀粉溶液作指示剂,滴定终点的现象是最后一滴标准溶液滴入溶液变蓝色且半分钟不变化.
分析 (1)氢氧化钠应该盛放在碱式滴定管中,根据碱式滴定管的排气泡法进行判断;
根据关系式2NaOH~H2SO4~SO2及氢氧化钠的物质的量计算出二氧化硫的质量,再计算出该葡萄酒中的二氧化硫含量;
(2)由于蒸馏时盐酸易挥发,消耗盐酸增多,该测定结果比实际值高;
Ⅰ、依据溶度积常数计算离子浓度;
Ⅱ、改用0.01000mol•L-1标准I2溶液滴定,选择淀粉溶液做指示剂,滴入最后一滴溶液变蓝色半分钟不变化证明反应达到终点;
空气氧化作用消耗标准溶液体积减小,测定结果偏低.
解答 解:(1)氢氧化钠溶液为碱性溶液,应该使用碱式滴定管,碱式滴定管中排气泡的方法:把滴定管的胶头部分稍微向上弯曲,再排气泡,所以排除碱式滴定管中的空气用c的方法;
根据2NaOH~H2SO4~SO2可知SO2的质量为:$\frac{1}{2}$×(0.0400mol/L×0.025L)×64g/mol=0.032g,该葡萄酒中的二氧化硫含量为:$\frac{0.032g}{0.1L}$=0.32g/L,
故答案为:c;0.32;
(2)由于蒸馏时盐酸易挥发,测定过程中消耗盐酸量增多,所以该测定结果比实际值高;
故答案为:偏高;
Ⅰ、当观察到出现淡红色沉淀且不再消失时停止滴定,若此时Cl-恰好沉淀完全即溶液中残余c(Cl-)=1.0×10-5 mol•L-1,c(Ag+)=$\frac{Ksp}{c(Cl{\;}^{-})}$=$\frac{2×10{\;}^{-10}}{1.0×10{\;}^{-5}}$=2.0×10-5mol/L,则此时溶液中的c(CrO42-)=$\frac{Ksp}{c{\;}^{2}(Ag{\;}^{+})}$=$\frac{1.12×10{\;}^{-12}}{(2.0×10{\;}^{-5}){\;}^{2}}$=2.8×10-3mol•L-1;
故答案为:2.8×10-3;
Ⅱ、改用0.01000mol•L-1标准I2溶液滴定,可选择淀粉溶液做指示剂,滴定终点的现象是:滴入最后一滴溶液变蓝色半分钟不变化证明反应达到终点;
故答案为:淀粉溶液;最后一滴标准溶液滴入溶液变蓝色且半分钟不变化.
点评 本题为考查了探究物质的组成、测量物质的含量的方法,题目难度中等,试题涉及了二氧化硫性质、中和滴定的计算,要求学生掌握探究物质组成、测量物质含量的方法,明确二氧化硫的化学性质及中和滴定的操作方法及计算方法,试题培养了学生灵活应用所学知识的能力.

 字词句段篇系列答案
字词句段篇系列答案| A. | 10Q | B. | 5Q~10Q | C. | 3Q | D. | 8Q |
| A. | 葡萄吃起来是酸的,故它属于酸性食物 | |
| B. | 正常人的人体内体液pH总保持恒定 | |
| C. | 食物的酸碱性与化学上所指溶液的酸碱性不同的 | |
| D. | 蛋白质在体内经消化后生成碳酸、硫酸、尿酸等,故它属于酸性食物 |
| t/min | 2 | 4 | 6 | 8 | 10 |
| n(A)/mol | 0.16 | 0.13 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率ν(C)=0.02 mol•L-1•min-1 | |
| B. | 平衡后降低温度,反应达到新平衡前ν(逆)>ν(正) | |
| C. | 其他条件不变,10 min后再充入一定量的A,平衡正向移动,A的转化率变小 | |
| D. | 保持其他条件不变,反应在恒压下进行,平衡时A的体积分数与恒容条件下反应相同 |
| A. | 2.7g金属铝变成铝离子时失去的电子数目为0.2NA | |
| B. | 16g CH4与18 g NH4+ 所含质子数相等 | |
| C. | 标准状况下,22.4 L汽油所含的分子数为NA | |
| D. | 在0℃,1.01×105Pa时,11.2L氮气所含的原子数目为NA |
| A. | 因亚硝酸钠有剧毒,所以不能用作食品添加剂 | |
| B. | 可用淀粉-KI试纸来鉴别一种盐溶液是亚硝酸钠还是氯化钠 | |
| C. | 能用硝酸银溶液来区别亚硝酸钠与氯化钠 | |
| D. | 因NaNO2具有较强的氧化性,可用酸性KMnO4溶液和FeCl2溶液鉴别NaCl与NaNO2 |
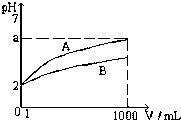 T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示
T℃时,pH=2的CH3COOH和H2SO4溶液各1mL,分别加水稀释到1000mL,其溶液的pH与溶液体积(V)的关系如图所示