题目内容
4.下表是元素周期表的一部分,其中每个数字序号代表一种短周期元素.
请按要求回答下列问题:
(1)写出②的元素名称氧;
(2)将①、②和③三种元素相比较,原子半径最大的是C(填元素符号);
(3)含有④元素的化合物在无色火焰上灼烧时火焰呈黄色;
(4)⑥元素的原子结构示意图为
 .
.
分析 (1)由元素在周期表中位置,可知①为C、②为O、③为F、④为Na、⑤为Mg、⑥为Al、⑦为S;
(2)同周期自左而右原子半径减小;
(3)钠元素焰色反应呈黄色;
(4)⑥为Al,原子核外电子数为13,有3个电子层,各层电子数为2、8、3.
解答 解:由元素在周期表中位置,可知①为C、②为O、③为F、④为Na、⑤为Mg、⑥为Al、⑦为S.
(1)②为氧元素,故答案为:氧;
(2)同周期自左而右原子半径减小,故原子半径:C>O>F,故答案为:C;
(3)④为Na钠元素,钠的化合物在无色火焰上灼烧时火焰呈黄色,故答案为:黄;
(4)⑥为Al,原子核外电子数为13,有3个电子层,各层电子数为2、8、3,原子结构示意图为 ,故答案为:
,故答案为: .
.
点评 本题考查元素周期表与元素周期律,比较基础,旨在考查学生对基础知识的理解掌握.

练习册系列答案
相关题目
14. 某同学在研究前18号元素时发现,可以将它们按原子序数递增的顺序排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素..
某同学在研究前18号元素时发现,可以将它们按原子序数递增的顺序排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素..
(1)图中a~f六中元素所形成的气态氢化物最稳定的是HF(填分子式)
(2)f在元素周期表中的位置是第三周期ⅣA族
(3)据图判断下列说法中错误的是AD
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.a、c两种元素组成的化合物中可能含有共价键
D.单质与水反应的剧烈程度:e>d>c
(4)b、c、d形成的简单离子,半径由大到小的顺序是F->Na+>Mg2+(用离子符号表示)
(5)共价键的性质通常用键长、键能等参数来描述,下表为部分非金属元素与氢元素形成共价键的键长与键能数据:
根据表中数据,归纳共价键键能与键长关系的一般规律同主族元素原子与相同其他原子形成的共价键,键长越短,键能越大.
 某同学在研究前18号元素时发现,可以将它们按原子序数递增的顺序排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素..
某同学在研究前18号元素时发现,可以将它们按原子序数递增的顺序排成如图所示的“蜗牛”形状,图中每个“•”代表一种元素,其中O点代表氢元素..(1)图中a~f六中元素所形成的气态氢化物最稳定的是HF(填分子式)
(2)f在元素周期表中的位置是第三周期ⅣA族
(3)据图判断下列说法中错误的是AD
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族
C.a、c两种元素组成的化合物中可能含有共价键
D.单质与水反应的剧烈程度:e>d>c
(4)b、c、d形成的简单离子,半径由大到小的顺序是F->Na+>Mg2+(用离子符号表示)
(5)共价键的性质通常用键长、键能等参数来描述,下表为部分非金属元素与氢元素形成共价键的键长与键能数据:
| 共价键 | H-F | H-Cl | H-O | H-S | H-N | H-P |
| 键长(pm) | 92 | 127 | 98 | 135 | 101 | 321 |
| 键能(kJ•mol-1) | 568 | 432 | 464 | 364 | 391 | 142 |
19.下列物质的水溶液能与铁发生置换反应的是( )
| A. | 碳酸钠 | B. | 硫酸铜 | C. | 硝酸钾 | D. | 氯化镁 |
16.锂-碘电池可用来为心脏起能源,其电池反应可简化为:2Li+I2═2LiI.下列有关说法正确的是( )
| A. | I2发生氧化反应 | B. | 碘电极为该电池的负极 | ||
| C. | 正极反应为:Li-e-═Li+ | D. | 该电池放电时化学能转化为电能 |
 )分子的一氯代物有2种.
)分子的一氯代物有2种. 系统命名为3-甲基-2-乙基-1-丁烯
系统命名为3-甲基-2-乙基-1-丁烯 请写出其单体结构:
请写出其单体结构: 、
、 、
、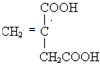 .
. ,在过氧化钠晶体中阴、阳离子的个数比为1:2;
,在过氧化钠晶体中阴、阳离子的个数比为1:2; (1)在一定条件下,对于密闭容器中进行的可逆反应:2HI (g)?H2(g)+I2(g),下列说法中,能说明这一反应已经达到化学反应限度的是D
(1)在一定条件下,对于密闭容器中进行的可逆反应:2HI (g)?H2(g)+I2(g),下列说法中,能说明这一反应已经达到化学反应限度的是D

 .
. .
. .
.